题目内容
1.已知:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-12CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ•mol-1
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列说法正确的是( )
| A. | H2(g)的燃烧热为285.8 kJ•mol-1 | |
| B. | 同质量的H2 (g)和CH3OH(l)完全燃烧,CH3OH(l)放出的热量多 | |
| C. | $\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)═$\frac{1}{2}$BaSO4(s)+H2O(l)△H=-57.3 kJ•mol-1 | |
| D. | 3H2(g)+CO2(g)=CH3OH(l)+H2O(l)△H=+135.9 kJ•mol-1 |
分析 A.根据燃烧热的定义判断;
B.分别计算物质的量,结合反应计算放出的热量;
C.有硫酸钡沉淀生成,放出热量大于57.3 kJ;
D.可结合盖斯定律计算反应热,并写出热化学方程式.
解答 解:A.燃烧热为1mol纯净物燃烧放热的热量,由2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1可知H2(g)的燃烧热为285.8kJ•mol-1,故A正确;
B.令H2(g)和CH3OH(l)的质量都为1g,则1g氢气燃烧放热为$\frac{1}{2}$×$\frac{1}{2}$×571.6=142.45KJ,1gCH3OH燃烧放热为$\frac{1}{32}$×$\frac{1}{2}$×1452=22.68KJ,所以H2(g)放出的热量多,故B错误;
C.有硫酸钡沉淀生成,放出热量大于57.3 kJ,则$\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)═$\frac{1}{2}$BaSO4(s)+H2O(l)△H<-57.3 kJ•mol-1,故C错误;
D.①2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
②2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1 452kJ•mol-1
按盖斯定律计算①×3-②得到6H2(g)+2CO2(g)═2CH3OH(l)+2H2O(l)△H=-262.8 kJ•mol-1.可知正确的是3H2(g)+CO2(g)═CH3OH(l)+H2O(l)△H=-131.4 kJ•mol-1,故D错误.
故选A.
点评 本题考查了热化学方程式和盖斯定律计算应用,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握燃烧热,中和热概念的理解应用,题目难度中等.

 发散思维新课堂系列答案
发散思维新课堂系列答案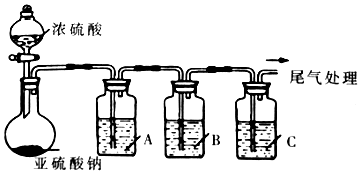
(1)实验可选用的实验试剂有浓硫酸、Na2SO3固体、Na2S溶液、BaCl2溶液、FeCl3溶液、品红溶液等.
①请完成下列表格
| 试剂 | 作用 | |
| A | 验证SO2的还原性 | |
| B | Na2S溶液 | |
| C | 品红溶液 |
③在上述装置中通入过量的SO2,为了验证A中发生了氧化还原反应,取A中溶液分成两份,并设计了如下实验:
方案一:往第一份试液中加入少量酸化的KMnO4溶液,紫红色褪去.该方案是否合理否.(填“是”或“否”)
方案二:往第二份试液中加入K3[Fe(CN)6]溶液,实验现象为生成蓝色沉淀.
④该小组将SO2通入酸化的高锰酸钾溶液中,再向溶液中滴加氯化钡溶液,发现有白色沉淀生成,说明SO2具有还原性.该方案的不妥之处可能为高锰酸钾用硫酸酸化.
(2)该兴趣小组利用“直接碘量法”对葡萄酒中的SO2进行测量.取50.00ml葡萄酒样品于250mL碘量瓶中.加入少量碎冰块,再加入1mL淀粉指示液,10mL硫酸溶液,用浓度为cmol/L的碘标准滴定溶液迅速滴定至淡蓝色,保持30s不变即为终点,记下消耗碘标准滴定溶液的体积为VmL.以水代替样品,做空白试验,操作同上,空白试验消耗碘标准滴定溶液的体积为Voml.该葡萄酒中SO2含量计算式为$\frac{c(V-{V}_{0})×64}{50}$g/L.
| A. | NH3既是氧化剂又是还原剂 | B. | 氢元素既被氧化又被还原 | ||
| C. | 0.5mol氢气生成时转移1mol电子 | D. | 镁具有氧化性 |
| A. | 天然气 | B. | 生物质能 | C. | 煤 | D. | 石油 |
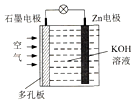 锌一空气电池(原理如图)适宜用作城市电动车的动力电源.该电池放电时Zn转化为ZnO.该电池工作时,下列说法正确的是( )
锌一空气电池(原理如图)适宜用作城市电动车的动力电源.该电池放电时Zn转化为ZnO.该电池工作时,下列说法正确的是( )| A. | Zn电极是该电池的正极 | |
| B. | Zn电极的电极反应:Zn+H2O-2e-═ZnO+2H+ | |
| C. | OH-向石墨电极移动 | |
| D. | 氧气在石墨电极上发生还原反应 |
| A. | 焰色反应是黄色 | |
| B. | 溶液有咸味 | |
| C. | 取少量溶液于试管中,滴加稀硝酸酸化的硝酸银溶液,出现白色沉淀 | |
| D. | 既出现A中的现象,又出现C中的现象 |
| A. | “雾”是微小水滴或冰晶组成的气溶胶系统 | |
| B. | “霾”中的灰尘对大气中的有害物质起吸附作用 | |
| C. | 雾霾中的二氧化硫、氮氧化物主要来自于化石燃料的燃烧 | |
| D. | 雾霾中的有机碳氢化合物主要来自于生物质的燃烧 |
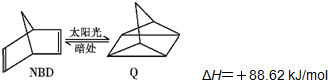 ,下列有关说法正确的是( )
,下列有关说法正确的是( )| A. | NBD和Q二者互为同分异构体 | |
| B. | 物质NBD的分子式为C7H7 | |
| C. | 物质Q的一氯取代物有2种 | |
| D. | 一定条件下,1molNBD最多可与2molBr2发生加成反应 |