题目内容
下列实验操作中错误的是( )
| A、用丁达尔效应区别FeCl3溶液与Fe(OH)3胶体 |
| B、可用加热分解的方法区别Na2CO3和NaHCO3固体 |
| C、分液时,先将分液漏斗中上层液体从上口倒出,再将下层液体从下口放出 |
| D、蒸馏时,温度计水银球靠近蒸馏烧瓶的支管口处,且冷却水从冷凝管的下口通入上口流出 |
考点:物质的检验和鉴别的实验方案设计,蒸馏与分馏,分液和萃取
专题:实验评价题
分析:A、溶液不具有丁达尔效应,但是胶体具有;
B、加热Na2CO3固体不分解,但是加热NaHCO3固体受热分解得到碳酸钠、水以及二氧化碳气体;
C、分液漏斗中中下层液体从下口放出,然后上层液体从上口倒出;
D、蒸馏时,温度计测定的是蒸汽温度,为保证气体冷凝充分,冷凝管中的水是下口进上口出.
B、加热Na2CO3固体不分解,但是加热NaHCO3固体受热分解得到碳酸钠、水以及二氧化碳气体;
C、分液漏斗中中下层液体从下口放出,然后上层液体从上口倒出;
D、蒸馏时,温度计测定的是蒸汽温度,为保证气体冷凝充分,冷凝管中的水是下口进上口出.
解答:
解:A、溶液不具有丁达尔效应,但是胶体具有,用丁达尔效应可以区别FeCl3溶液与Fe(OH)3胶体,故A正确;
B、加热Na2CO3固体不分解,但是加热NaHCO3固体受热分解得到碳酸钠、水以及二氧化碳气体,可用加热分解的方法区别Na2CO3和NaHCO3固体,故B正确;
C、使用分液漏斗时,分液漏斗中中下层液体从下口放出,然后上层液体从上口倒出,故C错误;
D、蒸馏时,温度计测定的是蒸汽温度,温度计水银球靠近蒸馏烧瓶的支管口处,为保证气体冷凝充分,冷凝管中的水是下口进上口出,故D正确.
故选C.
B、加热Na2CO3固体不分解,但是加热NaHCO3固体受热分解得到碳酸钠、水以及二氧化碳气体,可用加热分解的方法区别Na2CO3和NaHCO3固体,故B正确;
C、使用分液漏斗时,分液漏斗中中下层液体从下口放出,然后上层液体从上口倒出,故C错误;
D、蒸馏时,温度计测定的是蒸汽温度,温度计水银球靠近蒸馏烧瓶的支管口处,为保证气体冷凝充分,冷凝管中的水是下口进上口出,故D正确.
故选C.
点评:本题是一道物质的鉴别和检验方案的题目,注意仪器的使用以及物质的性质是解题的关键,难度中等.

练习册系列答案
相关题目
为达到预期的实验目的,下列操作正确的是( )
| A、预制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
| B、用碘的水溶液鉴别乙醇、四氯化碳 |
| C、欲配制质量分数为10%的CuSO4溶液,将10gCuSO4?5H2O溶解在90g水中 |
| D、某同学用托盘天平称量5.85gNaCl固体 |
下列溶液分pH一定小于7的是( )
| A、等体积的盐酸和氨水的混合液 |
| B、水电离出的c(OH-)=1×10-3mol?L-1的溶液 |
| C、80℃时的氯化钠溶液 |
| D、c(H+)=1×10-3mol?L-1的酸雨c(OH-)=1×10-3mol?L-1的碱等体积混合液 |
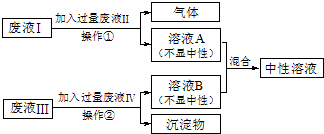
某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+.将溶液滴在蓝色石蕊试纸上,试纸变红.取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀.下列判断合理的是( )
| A、一定有SO42-、Cl- |
| B、一定有SO42-、Al3+ |
| C、可能含有Al3+、Na+ |
| D、一定没有CO32-、Cl-、Na+ |
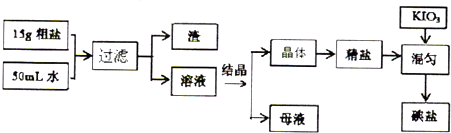
海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.下列有关说法不正确的是
( )

( )

| A、在精盐制备纯碱时,一定要先通氨气到饱和,再通二氧化碳到饱和 |
| B、在第②步骤中,溴元素被氧化 |
| C、用氢氧化钡溶液可鉴别NaHCO3和Na2CO3 |
| D、制取NaHCO3的反应是利用其溶解度小于NaCl |
下列物质属于非电解质的是( )
| A、C2H5OH |
| B、CaCl2 |
| C、H2SO4 |
| D、金属铜 |