题目内容
(本题7个空,每空2分,共14分)
(1)9.5g MgCl2溶于水配成100mL溶液,所得溶液的物质的量浓度为 ,取溶液25.0mL,稀释到500mL,此时溶液中Cl-的物质的量浓度为 ,在这两个实验中除了用烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是 。
(2)在反应3Cl2 + 6KOH(浓) == 5KCl + KClO3 + 3H2O中,氧化产物与还原产物的物质的量之比为 ,3molCl2参加该反应时,反应中转移 mol电子。
(3)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3- +4H++3e- = NO↑+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
①写出该氧化还原反应的化学方程式(不需要配平): 。
②反应中硝酸体现了 的性质。
(1)1mol·L-1,0.1mol·L-1,玻璃棒、100mL容量瓶。
(2)1:5,5。
(3)①Cu2O+HNO3(稀)——Cu(NO3)2+NO↑+H2O。
②氧化性和酸性。
【解析】
试题分析:(1)9.5g MgCl2的物质的量n= =
= =0.1mol,配成100mL溶液根据公式C=
=0.1mol,配成100mL溶液根据公式C=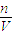 =
= =1mol/L;取配得的Mg Cl2溶液25.0mL,稀释到500mL,也就是将原溶液稀释20倍,所以,此时MgCl2的浓度为
=1mol/L;取配得的Mg Cl2溶液25.0mL,稀释到500mL,也就是将原溶液稀释20倍,所以,此时MgCl2的浓度为 =0.05mol/L,所得Mg Cl2溶液中Cl-的物质的量浓度为MgCl2浓度的两倍为0.1mol/L。还需用到的玻璃仪器是玻璃棒、100mL容量瓶。(2) 该反应中Cl2既是氧化剂又是还原剂。化合价升高为的氯原子对应的产物KCO3是氧化产物,化合价降为的氯原子生成的产物KCl是还原产物,其物质的量之比为1:5。3molCl2参加该反应时,生成1mol KClO3,Cl元素化合价升高5价,则转移电子5mol。(3) ①硝酸具有氧化性,题目提供的四种物质中只有Cu2O具有还原性,所以反应的方程式为硝酸与Cu2O反应生成硝酸铜、NO与水,反应方程式为:14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O,②反应中硝酸中氮元素存在硝酸铜、NO中,硝酸铜中氮元素化合价不变,硝酸表现酸性,NO中氮元素化合价降低,硝酸表现氧化性。
=0.05mol/L,所得Mg Cl2溶液中Cl-的物质的量浓度为MgCl2浓度的两倍为0.1mol/L。还需用到的玻璃仪器是玻璃棒、100mL容量瓶。(2) 该反应中Cl2既是氧化剂又是还原剂。化合价升高为的氯原子对应的产物KCO3是氧化产物,化合价降为的氯原子生成的产物KCl是还原产物,其物质的量之比为1:5。3molCl2参加该反应时,生成1mol KClO3,Cl元素化合价升高5价,则转移电子5mol。(3) ①硝酸具有氧化性,题目提供的四种物质中只有Cu2O具有还原性,所以反应的方程式为硝酸与Cu2O反应生成硝酸铜、NO与水,反应方程式为:14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O,②反应中硝酸中氮元素存在硝酸铜、NO中,硝酸铜中氮元素化合价不变,硝酸表现酸性,NO中氮元素化合价降低,硝酸表现氧化性。
考点:考查配制一定物质的量浓度的溶液,氧化还原反应。

下列表格中除去括号内的杂质,所选试剂和操作方法均正确的是
A | KCl(BaCl2) | 加过量K2CO3溶液后过滤,再蒸干滤液。 |
B | NaNO3(AgNO3) | 加足量NaCl溶液后过滤,再蒸馏滤液。 |
C | NaCl溶液(I2) | 加足量酒精后萃取分液 |
D | KNO3溶液(CCl4) | 直接进行分液操作。 |
 CH3COO-+H+,要使溶液中
CH3COO-+H+,要使溶液中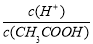 值增大,可以采取的措施是
值增大,可以采取的措施是 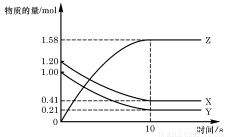
 Z(g)
Z(g) NH3↑ + H2O
NH3↑ + H2O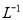
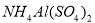 溶液中,滴加等浓度
溶液中,滴加等浓度 溶液x mL,下列叙述正确的是
溶液x mL,下列叙述正确的是 、
、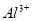 、
、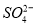 ,且
,且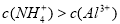
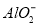 、
、
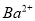 、
、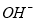 ,且
,且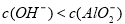
 .
.