题目内容
下表是A、B、C、D、E五种有机物的有关信息;
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为: ;写出在一定条件下,A生成高分子化合物的化学反应方程式 ;
(2)写出B在浓硫酸作用下,与浓硝酸反应的化学方程式: ;B具有的性质是 (填序号):①无色无味液体 ②无毒 ③不溶于水,密度比水大 ④任何条件下不与氢气反应 ⑤能与酸性KMnO4溶液反应,并使之褪色 ⑥因发生取代反应而使溴水褪色
(3)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为: ;
(4)写出由C氧化生成D的化学反应方程式: .
| A | B | C | D | E |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为: 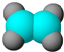 ③能与水在一定条件下反应生成C | ①由C、H两种元素组成; ②球棍模型为: 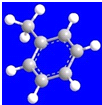 | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与E反应生成相对分子质量为100的酯. | ①相对分子质量比C少2; ②能由C氧化而成; | ①由C、H、O三种元素组成; ②球棍模型为: 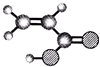 |
(1)A与溴的四氯化碳溶液反应的生成物的名称为:
(2)写出B在浓硫酸作用下,与浓硝酸反应的化学方程式:
(3)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为:
(4)写出由C氧化生成D的化学反应方程式:
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A能使溴水褪色说明含有碳碳双键或三键,结合其比例模型,可知A为CH2=CH2;A能和水反应生成C,C由C、H、O三种元素组成,能与Na反应,则C为CH3CH2OH;E的水溶液能使紫色石蕊试液变红,说明E为羧酸,乙醇与E反应生成相对分子质量为100的酯,结合E的球棍模型可知,则E为CH2=CHCOOH;B仅由C、H两种元素元素,结合其球棍模型,可知B是 ;D的相对分子质量比C少2,且能由C催化氧化得到,所以D是CH3CHO,据此解答.
;D的相对分子质量比C少2,且能由C催化氧化得到,所以D是CH3CHO,据此解答.
 ;D的相对分子质量比C少2,且能由C催化氧化得到,所以D是CH3CHO,据此解答.
;D的相对分子质量比C少2,且能由C催化氧化得到,所以D是CH3CHO,据此解答.解答:
解:A能使溴水褪色说明含有碳碳双键或三键,结合其比例模型,可知A为CH2=CH2;A能和水反应生成C,C由C、H、O三种元素组成,能与Na反应,则C为CH3CH2OH;E的水溶液能使紫色石蕊试液变红,说明E为羧酸,乙醇与E反应生成相对分子质量为100的酯,结合E的球棍模型可知,则E为CH2=CHCOOH;B仅由C、H两种元素元素,结合其球棍模型,可知B是 ;D的相对分子质量比C少2,且能由C催化氧化得到,所以D是CH3CHO,
;D的相对分子质量比C少2,且能由C催化氧化得到,所以D是CH3CHO,
(1)A为CH2=CH2,与溴的四氯化碳溶液反应生成BrCH2CH2Br,生成物的名称是:1,2-二溴乙烷,乙烯发生加聚反应生成高分子化合物,反应方程式为:n CH2=CH2
 ,
,
故答案为:1,2-二溴乙烷;n CH2=CH2
 ;
;
(2)B是 ,在浓硫酸作用下,与浓硝酸反应的化学方程式:
,在浓硫酸作用下,与浓硝酸反应的化学方程式: ,
,
甲苯是无色有特殊气味的、不溶于水且密度小于水的有毒液体,和酸性KMnO4溶液发生氧化反应,不能溴水都不反应,在催化剂条件下可与氢气发生加成反应,故选⑤,
故答案为: ;⑤;
;⑤;
(3)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为:CH2=CH-COOH+CH3CH2OH CH2=CH-COOCH2CH3+H2O,
CH2=CH-COOCH2CH3+H2O,
故答案为:CH2=CH-COOH+CH3CH2OH CH2=CH-COOCH2CH3+H2O;
CH2=CH-COOCH2CH3+H2O;
(4)由C氧化生成D的化学反应方程式:2CH3CH2OH+O2
2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O.
 ;D的相对分子质量比C少2,且能由C催化氧化得到,所以D是CH3CHO,
;D的相对分子质量比C少2,且能由C催化氧化得到,所以D是CH3CHO,(1)A为CH2=CH2,与溴的四氯化碳溶液反应生成BrCH2CH2Br,生成物的名称是:1,2-二溴乙烷,乙烯发生加聚反应生成高分子化合物,反应方程式为:n CH2=CH2
| 催化剂 |
| △ |
 ,
,故答案为:1,2-二溴乙烷;n CH2=CH2
| 催化剂 |
| △ |
 ;
;(2)B是
 ,在浓硫酸作用下,与浓硝酸反应的化学方程式:
,在浓硫酸作用下,与浓硝酸反应的化学方程式: ,
,甲苯是无色有特殊气味的、不溶于水且密度小于水的有毒液体,和酸性KMnO4溶液发生氧化反应,不能溴水都不反应,在催化剂条件下可与氢气发生加成反应,故选⑤,
故答案为:
 ;⑤;
;⑤;(3)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为:CH2=CH-COOH+CH3CH2OH
 CH2=CH-COOCH2CH3+H2O,
CH2=CH-COOCH2CH3+H2O,故答案为:CH2=CH-COOH+CH3CH2OH
 CH2=CH-COOCH2CH3+H2O;
CH2=CH-COOCH2CH3+H2O;(4)由C氧化生成D的化学反应方程式:2CH3CH2OH+O2
| Cu |
| △ |
故答案为:2CH3CH2OH+O2
| Cu |
| △ |
点评:本题考查有机物的推断,难度不大,注意根据有机物的模型与性质进行推断,侧重对基础知识的巩固.

练习册系列答案
相关题目
某烷烃和烯烃的混合气体的密度是1.07g?L-1(标准状况),该烷烃和烯烃的体积比是4:1.这两种烃是( )
| A、CH4、C2H4 |
| B、C2H6、C2H4 |
| C、CH4、C4H8 |
| D、CH4、C3H6 |
2012年3月29日,武汉大学张俐娜教授因对“纤维素低温溶解”的开创性研究,获得2011年度安塞姆佩恩奖(国际上纤维素与可再生资源材料领域的最高奖).制备乙酸乙酯的绿色合成路线之一为:
下列说法不正确的是( )

下列说法不正确的是( )
| A、M的分子式为C6H12O6 |
| B、N的结构简式为CH3COOH |
| C、M可以发生水解反应 |
| D、乙酸乙酯和N均能和NaOH溶液发生反应 |
如图所示装置可用于( )


| A、用铜和稀硝酸反应制NO |
| B、用铜和浓硝酸反应制NO2 |
| C、用NH4Cl与浓NaOH溶液反应制NH3 |
| D、加热NaHCO3制CO2 |
下列实验所采取的方法正确的是( )
| A、除去苯中苯酚,加入溴水后过滤 |
| B、分离苯和溴苯,加水后分液 |
| C、除去乙酸乙酯中乙酸,加入饱和NaOH溶液,振荡静置后分液 |
| D、区别乙酸、乙醛、乙醇,加入Cu(OH)2悬浊液加热 |
若溶液中由水电离产生的 c(OH-)=1×10-14mol?L-1,满足此条件的溶液中一定能够大量共存的离子组是( )
| A、K+、NH4+、SO42-、NO3- |
| B、K+、Na+、Cl-、AlO2- |
| C、K+、Na+、Cl-、NO3- |
| D、Al3+、Na+、NO3-、Cl- |
 下面给出了四种烃A、B、C、D的相关信息:
下面给出了四种烃A、B、C、D的相关信息: