题目内容
可以用铁缸盛浓硫酸或浓硝酸,这是因为 .
考点:铁的化学性质
专题:元素及其化合物
分析:铁在常温下遇到浓硫酸或浓硝酸会发生钝化,以此解答该题.
解答:
解:铁在常温下遇到浓硫酸或浓硝酸会发生钝化,表面生成一层致密的氧化膜阻止反应的进一步进行,所以生活中常用铁制的容器来运输或盛装浓硫酸或浓硝酸,
故答案为:铁在常温下遇到浓硫酸或浓硝酸会发生钝化,表面生成一层致密的氧化膜阻止反应的进一步进行.
故答案为:铁在常温下遇到浓硫酸或浓硝酸会发生钝化,表面生成一层致密的氧化膜阻止反应的进一步进行.
点评:本题涉及化学在生活以及实验室中的应用知识,注意化学知识和实际的灵活应用,是现在考试的热点,难度不大.

练习册系列答案
相关题目
铋(Bi)在医药方面有重要应用.下列关于
Bi和
Bi的说法正确的是( )
209 83 |
210 83 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、0.2 mol/L与0.1mol/L 醋酸溶液中c(H+)之比>2:1 |
| B、向0.1 mol/L 醋酸钠溶液中加入适量盐酸,得到的中性溶液:c(Na+)>c(CH3COO-)>c(Cl-)=c(CH3COOH) |
| C、pH=4的H2S溶液与pH=10 的NaOH溶液等体积混合:c(Na+)>2c(S2- )+c(HS-) |
| D、已知0.1 mol/L的二元酸H2A溶液pH=4.0,则在NaHA溶液中一定有:2c(OH-)+c(A2-)=c(H2A)+2c(H+) |
根据表中信息,判断下列叙述中正确的是( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 产物 | 产物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KClO3 | 浓盐酸 | / | Cl2 |
| A、反应①中可能有一种或两种元素被氧化 |
| B、反应①中,当只有少量Cl2时,反应可表示为Cl2+Fe2+═Fe3++2Cl- |
| C、反应②中KClO3被氧化,HCl被还原 |
| D、若反应②的另一种产物是KCl,则反应过程中1molKClO3得到6mole- |
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、由水电离出来的c(H+)=10-12mol/L的溶液中:Na+、HCO3-、SO42-、K+ |
| B、使酚酞试液变红的溶液中:S2-、SO42-、SO32-、Na+ |
| C、pH=0的溶液中:Na+、K+、Fe2+、NO3- |
| D、pH=7的溶液中:Al3+、Cl-、SO42-、CO32- |
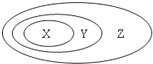 下表中所示物质或概念间的从属关系一定符合如图的是( )
下表中所示物质或概念间的从属关系一定符合如图的是( )