题目内容
下列说法正确的是( )
| A、离子晶体中可能含有共价键,一定含有金属元素 |
| B、分子晶体中可能不含共价键 |
| C、非极性分子中一定存在非极性键 |
| D、对于组成和结构相似的分子晶体,一定是相对分子质量越大,熔沸点越高 |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:A.离子晶体中可能不含金属元素;
B.分子晶体中可能含有共价键也可能不含共价键;
C.非极性分子中不一定存在非极性键;
D.氢键影响分子晶体的熔沸点.
B.分子晶体中可能含有共价键也可能不含共价键;
C.非极性分子中不一定存在非极性键;
D.氢键影响分子晶体的熔沸点.
解答:
解:A.离子晶体中可能不含金属元素,如铵盐,故A错误;
B.分子晶体中可能含有共价键也可能不含共价键,如稀有气体不含化学键,只含分子间作用力,故B正确;
C.非极性分子中不一定存在非极性键,如二氧化碳、甲烷等,故C错误;
D.对于组成和结构相似的分子晶体,不一定是相对分子质量越大,熔沸点越高,氢键影响物质的熔沸点,如水的熔沸点大于硫化氢,故D错误;
故选B.
B.分子晶体中可能含有共价键也可能不含共价键,如稀有气体不含化学键,只含分子间作用力,故B正确;
C.非极性分子中不一定存在非极性键,如二氧化碳、甲烷等,故C错误;
D.对于组成和结构相似的分子晶体,不一定是相对分子质量越大,熔沸点越高,氢键影响物质的熔沸点,如水的熔沸点大于硫化氢,故D错误;
故选B.
点评:本题考查了物质和化学键的关系,注意不能根据是否含有金属元素判断离子键,知道氢键对物质性质的影响,氢键不属于化学键,属于分子间作用力,为易错点.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
美国化学家研制出一种新型液态储氢材料,名叫硼氮-甲基环戊烷,它能在室温下安全工作,且在空气和水中也能保持稳定,这项技术进步为科学家们攻克现今制约氢经济发展的氢储存和运输难题提供了解决方案.下列说法正确的是( )
| A、该材料中只存在极性共价键 |
| B、其储氢与放氢过程中只发生物质的变化 |
| C、组成硼氮--甲基环戊烷的四种元素中氮的第一电离能最大 |
| D、甲基环戊烷核磁共振氢谱有3种峰,且峰面积比为3:4:4 |
下列各组微粒的空间构型相同的是( )
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2⑤CO2和C2H2 ⑥SiO44-和SO42-.
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2⑤CO2和C2H2 ⑥SiO44-和SO42-.
| A、全部 | B、除①④⑥以外 |
| C、③④⑤⑥ | D、②⑤⑥ |
下列实验装置或操作正确的是( )
| A | B | C | D |
 向容量瓶中转移液体 |  实验室制取乙酸乙酯 |  实验室制乙烯 |  分离酒精和水 |
| A、A | B、B | C、C | D、D |
分子式为C4HCl9的同分异构体共有(不考虑立体异构)( )
| A、4种 | B、5种 | C、6种 | D、8种 |
下列过程或现象与盐类水解无关的是( )
| A、纯碱溶液去油污 |
| B、明矾可用于净水 |
| C、加热稀醋酸溶液其pH值减小 |
| D、小苏打溶液与AlCl3溶液混合产生气体和沉淀 |
下列关于杂化轨道的叙述中,正确的是( )
| A、分子中的中心原子通过SP2杂化轨道成键时,该分子一定为平面三角形 |
| B、CH4分子中有四个完全相同的sp3-s6键 |
| C、杂化轨道只用于形成6键 |
| D、杂化轨道理论与VSEPR模型分析分子的空间构型结果常常相互矛盾 |
乙醇分子中不同的化学键如图所示,关于乙醇有关性质的说法不正确的是( )
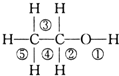

| A、和金属钠反应键①断裂 |
| B、在铜催化下和O2反应键①④断裂 |
| C、乙醇与金属钠反应比水与金属钠反应缓慢 |
| D、钠与乙醇反应时,钠熔化成一个小球在乙醇表面不断的游动 |
 (1)肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,1gN2H4在氧气中完全燃烧生成氮气和H2O,放出19.5kJ热量(25℃时),表示N2H4燃烧热的热化学方程式是
(1)肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,1gN2H4在氧气中完全燃烧生成氮气和H2O,放出19.5kJ热量(25℃时),表示N2H4燃烧热的热化学方程式是