题目内容
下列各组微粒的空间构型相同的是( )
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2⑤CO2和C2H2 ⑥SiO44-和SO42-.
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2⑤CO2和C2H2 ⑥SiO44-和SO42-.
| A、全部 | B、除①④⑥以外 |
| C、③④⑤⑥ | D、②⑤⑥ |
考点:判断简单分子或离子的构型
专题:化学键与晶体结构
分析:根据价层电子对互斥理论确定微粒空间构型,价层电子对个数=σ键+孤电子对个数,孤电子对个数=
×(a-xb),a为中心原子的价电子数,x为与中心原子结合的原子个数,b为与中心原子结合的原子最多能接受的电子数,据此判断.
| 1 |
| 2 |
解答:
解:①NH3中价层电子对个数=3+
×(5-3)=4且含有一个孤电子对,所以为三角锥形,H2O中价层电子对个数=
2+
×(6-2)=4且含有两个孤电子对,所以为V形结构,二者空间构型不同,故错误;
②NH4+中价层电子对个数是4且不含孤电子对,为正四面体形结构;H3O+中价层电子对个数都是3且含有一对孤电子对,所以为三角锥形结构,二者空间构型不同,故错误;
③NH3为三角锥形结构、H3O+为三角锥形结构,所以二者空间构型相同,故正确;
④O3、SO2中价层电子对个数都是3且都含有一对孤电子对,所以分子空间构型都是V形,故正确;
⑤CO2和C2H2分子都是直线型分子,故正确;
⑥SiO44-和SO42-中价层电子对个数都是4且不含孤电子对,所以空间构型都是正四面体结构,所以空间构型相同,故正确;
故选C.
| 1 |
| 2 |
2+
| 1 |
| 2 |
②NH4+中价层电子对个数是4且不含孤电子对,为正四面体形结构;H3O+中价层电子对个数都是3且含有一对孤电子对,所以为三角锥形结构,二者空间构型不同,故错误;
③NH3为三角锥形结构、H3O+为三角锥形结构,所以二者空间构型相同,故正确;
④O3、SO2中价层电子对个数都是3且都含有一对孤电子对,所以分子空间构型都是V形,故正确;
⑤CO2和C2H2分子都是直线型分子,故正确;
⑥SiO44-和SO42-中价层电子对个数都是4且不含孤电子对,所以空间构型都是正四面体结构,所以空间构型相同,故正确;
故选C.
点评:本题考查了微粒空间构型的判断,根据价层电子对理论解答即可,注意孤电子对个数=
×(a-xb)中各个字母的含义,阳离子时“( )”中数值要减去电荷数,阴离子时“( )”中数值要加上电荷数,为易错点,
| 1 |
| 2 |

练习册系列答案
相关题目
下列化合物中,在核磁共振氢谱图中有3种波峰的是( )
| A、甲酸乙酯 |
| B、丙酮(CH3COCH3) |
| C、乙醛 |
| D、丙烷 |
常温下,下列各组微粒在指定的分散系中一定能大量共存的是( )
| A、由水电离出的c(OH-)=1×10-13mol/L的溶液:Na+、Ba2+、Cl-、Br- |
| B、使甲基橙呈黄色的溶液:NO3-、I-、Na+、Cl- |
| C、含CO32-的溶液:Al3+、K+、Cl-、SO42- |
| D、鸡蛋清水溶胶:甲醛分子、蔗糖分子、甘油分子、Na+、Cl- |
下列化学用语使用正确的是( )
| A、N2的结构式:N=N |
B、H2O的比例模型: |
C、HClO的电子式: |
D、MgBr2的形成过程用电子式表示为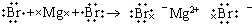 |
一定温度下,密闭体积的容器中进行反应4A(g)+6B(g)?4C(g)+5D(g),则下列有关化学反应速率的关系正确的是( )
| A、4v(A)=6v(B) | ||
| B、6v(B)=5v (D) | ||
C、v(C)=
| ||
D、v(A)=
|
下列说法正确的是( )
| A、离子晶体中可能含有共价键,一定含有金属元素 |
| B、分子晶体中可能不含共价键 |
| C、非极性分子中一定存在非极性键 |
| D、对于组成和结构相似的分子晶体,一定是相对分子质量越大,熔沸点越高 |
下列各组离子在指定溶液中,一定能大量共存的是( )
A、中性溶液中:Fe3+、Al3+、NO
| ||||||||
B、pH=11溶液中:CO
| ||||||||
C、由水电离的c(H+)=10-12mol?L-1的溶液中:Cl-、K+、NO
| ||||||||
D、加入甲基橙指示剂后显黄色的溶液中:Mg2+、NH
|
欲除去下列物质中混入的少量杂质(括号内物质为杂质),正确的是( )
| A、乙酸乙酯(乙酸):加入适量乙醇,充分反应 |
| B、乙醇(水):加入新制生石灰,蒸馏 |
| C、乙烷(乙烯):加入适量H2,适当条件下进行反应 |
| D、乙醇(乙酸):加入金属钠,蒸馏 |