题目内容
12.(1)指出下列实验用品或仪器(已经洗涤干净)使用时的第一步操作:①石蕊试纸(检验气体性质)将石蕊试纸润湿;
②容量瓶是否漏水.
(2)下列有关化学实验操作中“先”与“后”的说法正确的是ABCE(填代号).
A.用排水法收集气体后,先移出导管,后撤酒精灯
B.给试管加热时,先均匀加热,后局部加热
C.碱液流到桌子上,先用稀醋酸溶液中和,后用水洗
D.浓硫酸不慎洒到皮肤上,先迅速用水冲洗,后涂上3%-5%的NaHCO3溶液
E.点燃可燃性气体(如H2、CO、C2H4等)时,都要先检验气体纯度,后点燃.
分析 (1)①石蕊试纸检验气体需要湿润;
②容量瓶需要检查是否漏液;
(2)A.先移出导管,后撤酒精灯,可防止水倒流;
B.给试管加热时,先均匀加热,后局部加热,防止受热不均匀;
C.中和减低腐蚀性;
D.浓硫酸不能用水冲洗,稀释放出大量的热;
E.点燃可燃性气体(如H2、CO、C2H4等)时,若不纯易发生爆炸.
解答 解:(1)①石蕊试纸(检验气体性质)第一步操作为将石蕊试纸润湿,故答案为:将石蕊试纸润湿;
②容量瓶使用的第一步操作为检验容量瓶是否漏水,故答案为:是否漏水;
(2)A.先移出导管,后撤酒精灯,可防止水倒流试管炸裂,操作合理,故A正确;
B.给试管加热时,先均匀加热,后局部加热,防止受热不均匀,操作合理,故B正确;
C.碱液流到桌子上,先用稀醋酸溶液中和,后用水洗,减低腐蚀性,操作合理,故C正确;
D.浓硫酸不能用水冲洗,稀释放出大量的热,不能立即用水冲洗,先用布擦拭,再用水冲洗,后涂上3%-5%的NaHCO3溶液,故D错误;
E.点燃可燃性气体(如H2、CO、C2H4等)时,若不纯易发生爆炸,则先检验气体纯度,后点燃,故E正确;
故答案为:ABCE.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、实验基本操作、实验安全为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
13.仪器名称为“蒸馏烧瓶”的是( )
| A. |  | B. |  | C. |  | D. |  |
3.某酸性FeSO3溶液中含有少量的SnSO4,为得到纯净的硫酸亚铁晶体(FeSO4•xH2O),可向溶液中通入H2S气体至饱和,然后用硫酸酸化至pH=2,过滤后,将所得滤液蒸发浓缩、冷却结晶、过滤洗涤,得到硫酸亚铁晶体.查阅资料,得到相关物质的有关数据如表:
(1)用硫酸亚铁晶体配置FeSO4溶液时还需加入的物质是铁粉和稀硫酸;
(2)为检验制得的硫酸亚铁晶体中是否含有Fe3+,可选用的试剂为AC;
A.KSCN溶液B.稀硫酸C.淀粉-KI溶液D.KMnO4溶液
(3)通入H2S气体至饱和的目的是除去溶液中的Sn2+离子,并防止Fe2+被氧化;用硫酸酸化至pH=2的目的是防止Fe2+离子生成沉淀;
(4)为研究硫酸亚铁晶体的热分解,某兴趣小组同学称取ag硫酸亚铁晶体样品,按图1装置进行高温加热,使其完全分解(硫酸亚铁晶体在高温条件下回分解为三种化合物和一种单质,该单质能使带火星的木条复燃),对所得产物进行探究,并通过称量装置B的质量测出x的值.
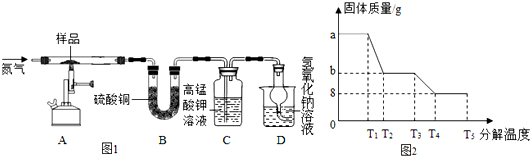
①装置B中午睡硫酸铜粉末变蓝,质量增加12.6g,说明产物中有水,装置C中高锰酸钾溶液褪色,说明产物中含有二氧化硫;
②实验中要持续通入氮气,否则测出的x会偏小(填“偏大”、“偏小”或“不变”);
③硫酸亚铁晶体完全分解后装置A中固体呈红棕色,将其加入足量稀盐酸中,固体全部溶解,得黄色溶液;
④某研究所利用SDTQ600热分析仪对硫酸亚铁晶体进行热分解,获得相关数据,绘制成的固体质量与分解温度的关系图如图2,根据图中有关数据,可计算出x为7.
| 25℃ | pH | 25℃ | pH |
| 饱和H2S溶液 | 3.9 | FeS开始沉淀 | 3.0 |
| SnS沉淀完全 | 1.6 | FeS沉淀完全 | 5.5 |
(2)为检验制得的硫酸亚铁晶体中是否含有Fe3+,可选用的试剂为AC;
A.KSCN溶液B.稀硫酸C.淀粉-KI溶液D.KMnO4溶液
(3)通入H2S气体至饱和的目的是除去溶液中的Sn2+离子,并防止Fe2+被氧化;用硫酸酸化至pH=2的目的是防止Fe2+离子生成沉淀;
(4)为研究硫酸亚铁晶体的热分解,某兴趣小组同学称取ag硫酸亚铁晶体样品,按图1装置进行高温加热,使其完全分解(硫酸亚铁晶体在高温条件下回分解为三种化合物和一种单质,该单质能使带火星的木条复燃),对所得产物进行探究,并通过称量装置B的质量测出x的值.

①装置B中午睡硫酸铜粉末变蓝,质量增加12.6g,说明产物中有水,装置C中高锰酸钾溶液褪色,说明产物中含有二氧化硫;
②实验中要持续通入氮气,否则测出的x会偏小(填“偏大”、“偏小”或“不变”);
③硫酸亚铁晶体完全分解后装置A中固体呈红棕色,将其加入足量稀盐酸中,固体全部溶解,得黄色溶液;
④某研究所利用SDTQ600热分析仪对硫酸亚铁晶体进行热分解,获得相关数据,绘制成的固体质量与分解温度的关系图如图2,根据图中有关数据,可计算出x为7.
20.下列溶液暴露于空气中,开始一段时间其pH变小的是(不考虑溶质挥发)( )
①H2S ②H2SO3③Na2S ④Ca(OH)2 ⑤氯水 ⑥Na2SO3.
①H2S ②H2SO3③Na2S ④Ca(OH)2 ⑤氯水 ⑥Na2SO3.
| A. | ①③④ | B. | ②⑤⑥ | C. | ①②④⑤ | D. | ②④⑤⑥ |
7.可用如图装置制取(必要时可加热)和收集的气体是( )
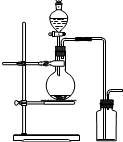

| A. | 氯酸钾溶液与二氧化锰反应制氧气 | B. | 浓氨水与氢氧化钙固体制氨气 | ||
| C. | 乙醇和浓硫酸(170℃)制乙烯 | D. | 铜和浓硝酸制二氧化氮 |
17.据报道,科学家已成功合成了少量的O4,有关O4的说法正确的是( )
| A. | O4的摩尔质量是64g | |
| B. | O4与O3、O2互为同位素 | |
| C. | 相同质量的O4与O3所含原子个数之比为1:1 | |
| D. | 32gO4所含的电子数为32NA(NA为阿伏加德罗常数) |
4.下列现象或事实不能用同一原理解释的是( )
| A. | 浓硝酸和氯水用棕色试剂瓶保存 | |
| B. | 硫化钠和硫酸亚铁固体长期暴露在空气中变质 | |
| C. | 常温下铁和铂都不溶于浓硝酸 | |
| D. | H2O2溶液中加入少量MnO2或FeCl3溶液都能增大反应速率 |
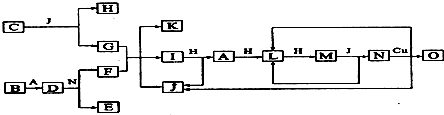
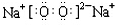 .
.