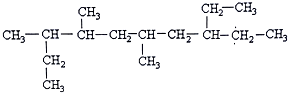题目内容
13.NA代表阿伏加德罗常数的值.下列叙述正确的是( )| A. | 78g过氧化钠中存在的共价价键总数为2NA | |
| B. | 22.4L(标准状况)氯气充分参与化学反应,转移的电子数不一定为2NA | |
| C. | 1 L0.1 mol•L-1的NaHS溶液中HS-、S2-和H2S粒子数之和小于0.1NA | |
| D. | 一定条件下,密闭容器中2molSO2与1molO2充分反应,产物的分子数为2NA |
分析 A、求出过氧化钠的物质的量,然后根据过氧化钠中存在1个共价键来分析;
B、氯气参与反应后的价态可能变为-1价,还可能变为+1价、+3价、+5价和+7价;
C、HS-在溶液中可以电离为S2-也可以水解为H2S;
D、二氧化硫和氧气的反应为可逆反应.
解答 解:A、78g过氧化钠的物质的量为1mol,而过氧化钠中存在1个共价键,故1mol过氧化钠中含1mol共价键,即NA个,故A错误;
B、氯气参与反应后的价态可能变为-1价,还可能变为+1价、+3价、+5价和+7价,故标况下22.4L氯气反应后转移的电子数不一定是2NA个,还可能是6NA个、10NA、14NA个,故B正确;
C、HS-在溶液中可以电离为S2-也可以水解为H2S,故HS-、S2-和H2S粒子数之和为0.1NA,故C错误;
D、二氧化硫和氧气的反应为可逆反应,故产物分子的个数小于2NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
1.已知A、B、C、D为短周期元素,A、D同主族,B、C、D同周期,A的气态氢化物的稳定性大于D的气态化物的稳定性,B、C为金属元素,B的阳离子的氧化性小于C的阳离子的氧化性.下列说法正确的是( )
| A. | A与B形成的化合物中只含离子键 | |
| B. | A的气态氢化物的沸点一定高于D的气态氢化物的沸点 | |
| C. | 若A与C的原子序数相差5,则二者形成化合物的化学式一定为C2A3 | |
| D. | 相同条件下,B的最高价氧化物的水化物的碱性比C的最高价氧化物的水化物的碱性强 |
8.某烃苯环上的一氯代物只有2种,则该烃是( )
| A. |  | B. |  | C. |  | D. |  |
2.W、X、Y、Z四种短周期元素在周期表中的相对位置如图所示.W、X、Y、Z原子的最外层电子数之和为21.下列说法中错误的是( )
| W | ||||
| X | Y | Z |
| A. | 元素X的单质能与强酸、强碱反应 | |
| B. | 简单阴离子的还原性:W>Z | |
| C. | 气态氢化物的稳定性:W>Y | |
| D. | 元素W、X与钠元素可形成化合物Na3XW6 |
3.人类的生存离不开燃料.未来社会最理想的燃料是( )
| A. | 煤 | B. | 石油 | C. | 天然气 | D. | 氢气 |
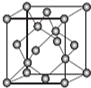 AIN是重要的半导体材料,Ga(镓)、P、As(砷)都是形成化合物半导体材料的重要元素.
AIN是重要的半导体材料,Ga(镓)、P、As(砷)都是形成化合物半导体材料的重要元素. CH3CH2COONH4+3NH3+2Ag+H2O.在此过程中丙醛发生氧化(氧化、还原)反应,此反应可以检验醛基的存在.
CH3CH2COONH4+3NH3+2Ag+H2O.在此过程中丙醛发生氧化(氧化、还原)反应,此反应可以检验醛基的存在. CH3COOC2H5+H2O.
CH3COOC2H5+H2O.