题目内容
1.已知A、B、C、D为短周期元素,A、D同主族,B、C、D同周期,A的气态氢化物的稳定性大于D的气态化物的稳定性,B、C为金属元素,B的阳离子的氧化性小于C的阳离子的氧化性.下列说法正确的是( )| A. | A与B形成的化合物中只含离子键 | |
| B. | A的气态氢化物的沸点一定高于D的气态氢化物的沸点 | |
| C. | 若A与C的原子序数相差5,则二者形成化合物的化学式一定为C2A3 | |
| D. | 相同条件下,B的最高价氧化物的水化物的碱性比C的最高价氧化物的水化物的碱性强 |
分析 A、B、C、D为短周期元素,A、D同主族,B、C、D同周期,A的气态氢化物的稳定性大于D的气态化物的稳定性,元素的非金属性越强,其气态氢化物越稳定,所以A的非金属性大于D,则A的原子序数小于D;
B、C为金属元素,B的阳离子的氧化性小于C的阳离子的氧化性,则B的原子序数小于C,D为非金属性元素,所以C的原子序数小于D,再结合原子结构、元素周期律分析解答.
解答 解:A、B、C、D为短周期元素,A、D同主族,B、C、D同周期,A的气态氢化物的稳定性大于D的气态化物的稳定性,元素的非金属性越强,其气态氢化物越稳定,所以A的非金属性大于D,则A的原子序数小于D;
B、C为金属元素,B的阳离子的氧化性小于C的阳离子的氧化性,则B的原子序数小于C,D为非金属性元素,所以C的原子序数小于D,
A.A可以为Cl元素,D可以为Al元素,二者形成的氯化铝为共价化合物,不存在离子键,故A错误;
B.若A为C、D为Si,二者形成的氢化物分别为甲烷和硅烷,甲烷的沸点小于硅烷,故B错误;
C.若A为N元素,C为Mg元素,二者的原子序数相差5,二者形成化合物的化学式可能为Mg3N2,化学式为Y3W2,故C错误;
D.由于B、C为相同周期的金属元素,且原子序数B小于C,则金属性B大于C,则相同条件下B的最高价氧化物的水化物的碱性比C的最高价氧化物的水化物的碱性强,故D正确;
故选D.
点评 本题考查了原子结构与元素周期律的综合应用,题目难度中等,推断各元素的相对位置为解答关键,注意掌握原子结构与元素周期律的关系,试题培养了学生的分析能力及逻辑推理能力.

练习册系列答案
相关题目
12.X、Y、Z、W均为短周期元素,且原子序数依次增大,X的单质为密度最小的气体,Y的原子最外层电子数是其周期数的三倍,Z与 X的原子最外层电子数相同,Y与 W的原子最外层电子数相同. 下列叙述正确的是( )
| A. | X、Y和 Z的原子半径大小顺序为 Y>Z>X | |
| B. | Z和 Y组成的化合物中一定既有离子键又有共价键. | |
| C. | 元素 X、Y、W各自最高和最低化合价的代数和分别为 0、4、4 | |
| D. | 同时含有 X、Y、Z、W四种元素的两种不同化合物能相互反应 |
9.下列有关分子晶体熔点的高低叙述中,正确的是( )
| A. | H2O<HF | B. | SiCl4>CCl4 | C. | HCl>HF | D. | N2>CO |
16.A、B、C、D、E是同周期的五种主族元素.A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A;C和D的最高价氧化物对应的水化物均呈酸性,且酸性C>D,E是这五种元素中简单离子半径最小的元素,它们的原子序数由小到大的顺序是( )
| A. | B<A<D<C<E | B. | E<B<A<D<C | C. | B<A<E<D<C | D. | E<D<C<B<A |
13.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 78g过氧化钠中存在的共价价键总数为2NA | |
| B. | 22.4L(标准状况)氯气充分参与化学反应,转移的电子数不一定为2NA | |
| C. | 1 L0.1 mol•L-1的NaHS溶液中HS-、S2-和H2S粒子数之和小于0.1NA | |
| D. | 一定条件下,密闭容器中2molSO2与1molO2充分反应,产物的分子数为2NA |
10.下列各组元素性质的比较中,正确的是( )
| A. | 电子层数:P<S<Cl | B. | 最高正化合价:N<O<F | ||
| C. | 原子半径:C<N<O | D. | 金属性:Na>Mg>Al |
11.下列关于电解KNO3溶液时的叙述正确的是( )
| A. | NO3-向阴极移动,K+向阳极移动,分别在对应的极上析出 | |
| B. | 随电解的进行,溶液的pH减小 | |
| C. | OH-向阳极移动,阳极附近溶液显碱性 | |
| D. | 阴极上H+得电子被还原成H2,促进水的电离平衡正向移动,富集下来的OH-使得阴极附近溶液呈碱性 |
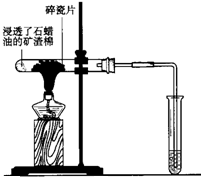 如图所示,将浸透了石蜡油的(17个碳原子以上的液态烷烃混合物)的石棉放置在硬质试管的底部,试管中加入碎瓷片,给碎瓷片加强热,石蜡油蒸汽通过炽热的碎瓷片表面发生反应,生成一定量的气体.利用该气体进行实验:
如图所示,将浸透了石蜡油的(17个碳原子以上的液态烷烃混合物)的石棉放置在硬质试管的底部,试管中加入碎瓷片,给碎瓷片加强热,石蜡油蒸汽通过炽热的碎瓷片表面发生反应,生成一定量的气体.利用该气体进行实验: