题目内容
下列物质属于纯净物的是( )
| A、纯净的食盐水 |
| B、冰水混合物 |
| C、干净的玻璃 |
| D、纯净的矿泉水 |
考点:混合物和纯净物
专题:物质的分类专题
分析:只由一种物质组成的属于纯净物,据此分析.
解答:
解:A、食盐水是氯化钠的水溶液,是混合物,故A不选;
B、冰即固态的水,故冰水混合物即水,是由一种物质构成的,故是纯净物,故B选;
C、玻璃的主要成分有二氧化硅、硅酸钠和硅酸钙,是混合物,故C不选;
D、矿泉水中除了主要成分是水外,还含有多种矿物质,故是混合物,故D不选.
故选B.
B、冰即固态的水,故冰水混合物即水,是由一种物质构成的,故是纯净物,故B选;
C、玻璃的主要成分有二氧化硅、硅酸钠和硅酸钙,是混合物,故C不选;
D、矿泉水中除了主要成分是水外,还含有多种矿物质,故是混合物,故D不选.
故选B.
点评:本题考查了纯净物的概念,应注意所谓的纯净物须是只由一种物质构成.难度不大.

练习册系列答案
相关题目
在一个密闭容器中充入1molCO2 和3molH2,在850℃时,气体混合物达到下式所示平衡:CO2+H2?CO+H2O.已知达到平衡时CO2的转化率为75%.那么当H2改为4mol,在上述条件下平衡时生成CO 和H2O的物质的量之和为( )
| A、1.5mol |
| B、1.8mol |
| C、1.6mol |
| D、2.5mol |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、等物质的量的N2和CO所含有的原子数均为2NA |
| B、通常状况下,64g SO2中含有的分子数为NA |
| C、标准状况下,22.4L CH4和O2的混合气体所含有的分子数为2NA |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
下列说法中正确的是( )
| A、1 L 水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L |
| B、从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L |
| C、配制500 mL 0.2 mol/L的CuSO4溶液,需称量CuSO4固体的质量为16.0g |
| D、中和100 mL 1 mol/L的H2SO4溶液,需NaOH的质量为4.0g |
下列说法不正确的是( )
| A、溶液、胶体和悬浊液这三种分散系的本质区别是能否透过滤纸或半透膜 |
| B、仅用新制的氢氧化铜悬浊液一种试剂可鉴别乙醇、甘油、乙醛、乙酸、乙酸乙酯、葡萄糖溶液(必要时可加热) |
C、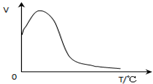 过氧化氢在酶催化作用下的分解反应速率随温度的变化关系如图所示 |
| D、工业上从海带中提取碘单质,经历的步骤有浸泡-过滤-氧化-结晶-粗碘提纯 |
甲乙两个装置中,胶头滴管中吸入某种液体,广口瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则所用试剂可能是( )

| A、甲:NaOH溶液和CO2,乙:H2O2和MnO2 |
| B、甲:CaCl2和Na2CO3溶液,乙:NaOH溶液和Cl2 |
| C、甲:浓硫酸和铝片.乙:浓氨水和SO2 |
| D、甲:浓硫酸和蔗糖.乙:水和氯化氢气体 |