题目内容
下列说法或表示方法中正确的是( )
| A、等质量的硫蒸气和硫黄分别完全燃烧,后者放出的热量多 |
| B、氢气的标准燃烧热为285.8 kJ?mol-1,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ?mol-1 |
| C、Ba(OH)2?8H2O(s)+2NH4Cl(s)═BaCl2(s)+2NH3(g)+10H2O(l)△H<0 |
| D、已知中和反应的反应热△H=-57.3 kJ?mol-1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量要大于57.3 kJ |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、硫蒸气所含能量比硫固体多;
B、据燃烧热大过年分析;
C、氯化铵和氢氧化钡反应吸热;
D、浓硫酸溶于水放热.
B、据燃烧热大过年分析;
C、氯化铵和氢氧化钡反应吸热;
D、浓硫酸溶于水放热.
解答:
解:A、硫蒸气比硫固体所含能量高,等质量的硫蒸气和硫黄分别完全燃烧,前者放出的热量多,故A错误;
B、燃烧热是指1mol可燃物燃烧放出的热量,热化学方程式中氢气是2mol,故B错误;
C、氯化铵和氢氧化钡反应吸热,△H>0,故C错误;
D、浓硫酸溶于水放热,故D正确;
故选D.
B、燃烧热是指1mol可燃物燃烧放出的热量,热化学方程式中氢气是2mol,故B错误;
C、氯化铵和氢氧化钡反应吸热,△H>0,故C错误;
D、浓硫酸溶于水放热,故D正确;
故选D.
点评:本题考查了焓变的求算、燃烧热、中和热、常见吸热反应,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
关于钠的叙述中,正确的是( )
| A、钠在空气中燃烧生成过氧化钠 |
| B、钠是银白色金属,硬度很大 |
| C、钠投入乙醇中,会浮在液面 |
| D、钠的保存要注意防水、防空气 |
已知草酸钠与高锰酸钾反应的化学方程式为:5Na2C2O4+2KMnO4+8H2SO4═l0CO2↑+2MnSO4+K2SO4+8H2O+5Na2SO4.下列有关说法中正确的是( )
| A、H2SO4含有离子键和共价键 |
| B、Na2C2O4被还原 |
| C、标准状况下,每转移l mol电子生成11.2L的混合气体 |
| D、CO2只含极性键 |
下列关于乙醇的说法正确的是( )
| A、用萃取分液的方法除去酒精中的水 |
| B、可由乙烯通过加成反应制取 |
| C、也可用来保存金属钠 |
| D、无水乙醇常用于医疗消毒 |
下列实验会产生所描述现象的是( )
| A、将SO2气体通入BaCl2溶液中,有白色沉淀产生 |
| B、将Na2CO3粉末加入新制饱和氯水中,有气体产生 |
| C、将铜片加入浓硫酸中加热,有红棕色气体产生 |
| D、将少量新制氯水加入KI溶液中,再加入CC14,振荡、静置后有紫色沉淀析出 |
下列物质中,存在非极性键的化合物的是( )
| A、NaOH |
| B、CH4 |
| C、H2 |
| D、Na2O2 |
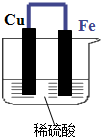 如图示的装置中
如图示的装置中