题目内容
6.常温下,将100mL0.05mol/L氢硫酸中逐渐通入氯气,下列叙述正确的是( )| A. | 溶液pH先变大后变小 | B. | 溶液导电能力逐渐增强 | ||
| C. | 氢硫酸完全反应生成1.6g硫 | D. | 这个反应可以证明还原性Cl->S2- |
分析 向100mL0.05mol/L氢硫酸中逐渐通入氯气,发生H2S+Cl2=2H++2Cl-+S↓,生成盐酸,酸性增强,若硫化氢完全反应,n(H2S)=0.005mol,则生成S为0.005mol,以此来解答.
解答 解:A.发生H2S+Cl2=2H++2Cl-+S↓,生成盐酸,酸性增强,pH在减小,故A错误;
B.硫化氢为弱电解质,生成HCl为强电解质,溶液中离子浓度增大,导电性增强,故B正确;
C.若硫化氢完全反应,n(H2S)=0.005mol,则生成S为0.005mol,其质量为0.005mol×32g/mol=0.16g,故C错误;
D.反应的离子方程式为H2S+Cl2=2H++2Cl-+S↓,还原剂的还原性大于还原产物的还原性,即还原性S2->Cl-,故D错误;
故选B.
点评 本题考查氯气的性质,为高频考点,把握发生的氧化还原反应为解答的关键,侧重分析能力与计算能力的考查,涉及pH、导电性、离子反应及计算等,综合性较强,题目难度不大.

练习册系列答案
相关题目
1.下列离子方程式中书写正确的是( )
| A. | 氢氧化钡溶液与稀硫酸混合:Ba2++SO42-→BaSO4↓ | |
| B. | 铁粉溶于稀硫酸中:2Fe+6H+→2Fe3++3H2↑ | |
| C. | 氨水与盐酸混合:OH-+H+→H2O | |
| D. | 硫化钠溶液中滴加硝酸银:S2-+2Ag+→Ag2S↓ |
17.能表示质量数是37的阴离子是( )
| A. | 19个质子,18个中子,19个电子 | B. | 18个质子,19个中子,18个电子 | ||
| C. | 19个质子,18个中子,18个电子 | D. | 17个质子,20个中子,18个电子 |
14.下列物质用途不正确的是( )
| A. | 重晶石可作钡餐与白色颜料 | |
| B. | 硫酸是重要的化工原料之一,可用来制造磷肥 | |
| C. | 明矾常用作消毒剂 | |
| D. | 胆矾可用于配置波尔多液 |
1.在标准状况下,相同物质的量的二氧化硫和三氧化硫具有相同的( )
| A. | 分子数 | B. | 密度 | C. | 质量 | D. | 体积 |
18.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 23gNO2和N2O4的混合气体中含原子总数为1.5NA | |
| B. | 31g白磷P4(如图)中所含的P-P键的个数为0.25NA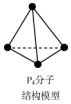 | |
| C. | 足量的Cu与100mL18.4mol/L的浓硫酸反应,失去3.68NA个电子 | |
| D. | 浓度均为2.0mol/L的盐酸和醋酸溶液各100mL,其含氢离子均为0.2NA |
15. 如图装置实验,一段时间后某同学记录如下:
如图装置实验,一段时间后某同学记录如下:
①Zn为正极,Cu为负极 ②屯解质溶液pH不变
③电子流动的方向为:Zn→Cu ④Cu极上有氢气产生
⑤若有1mol电子流过导线,则产生氢气11.2L.
上述记录中描述正确的是( )
 如图装置实验,一段时间后某同学记录如下:
如图装置实验,一段时间后某同学记录如下:①Zn为正极,Cu为负极 ②屯解质溶液pH不变
③电子流动的方向为:Zn→Cu ④Cu极上有氢气产生
⑤若有1mol电子流过导线,则产生氢气11.2L.
上述记录中描述正确的是( )
| A. | ③④⑤ | B. | ③④ | C. | ①②③ | D. | ②④⑤ |
10.①pH=3的CH3COOH溶液;②pH=3的HCl溶液;③pH=11的氨水;④pH=11的NaOH溶液.相同条件下,有关上述溶液的比较中,正确的是( )
| A. | 将②、③溶液混合后,pH=7,消耗溶液的体积:②<③ | |
| B. | 向溶液中加入100mL水后,溶液的pH:③>④>①>② | |
| C. | 等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 | |
| D. | 水电离产生的c(H+):①=②=③=④ |
 氮及其化合物在工农业生产中具有重要作用.
氮及其化合物在工农业生产中具有重要作用.