题目内容
t ℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)  2Z(g),各组分在不同时刻的浓度如下表:
2Z(g),各组分在不同时刻的浓度如下表:
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 2 min末浓度/mol·L-1 | 0.08 | a | b |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法正确的是
A.平衡时,X的转化率为20%
B.t ℃时,该反应的平衡常数为40
C.增大平衡后的体系压强, v正增大,v逆减小,平衡向正反应方向移动
D.前2 min内,用Y的变化量表示的平均反应速率v(Y)="0.03" mol·L-1·min-1
D
解析试题分析:根据三段式进行计算:X+3Y  2Z
2Z
初始浓度(mol?L?1) 0.1 0.2 0
转化浓度(mol?L?1)0.05 0.15 0.1
平衡浓度(mol?L?1)0.05 0.05 0.1
A、平衡时,X的转化率=0.05mol/L÷0.1mol/L×100%=50%,错误;B、平衡常数=0.12÷(0.05×0.053)=1600,错误;C、增大平衡后的体系压强,正反应速率、逆反应速率都增大,错误;D、前2 min内,用Y的变化量表示的平均反应速率v(Y) =3v(X)=3×(0.1mol?L?1-0.08mol?L?1)÷2min="0.03" mol·L-1·min-1,正确。
考点:本题考查化学平衡移动,转化率、平衡常数、反应速率的计算。

 阅读快车系列答案
阅读快车系列答案下列事实可用勒夏特列原理解释的是
| A.使用催化剂有利于加快合成氨反应的反应速率 |
| B.硫酸工业中,将黄铁矿粉碎后加入沸腾炉中 |
| C.500℃左右比在室温时更有利于提高合成氨的转化率 |
| D.配制氯化铁溶液时,将氯化铁加入盐酸中,然后加水稀释 |
某温度下,体积一定的密闭容器中进行如下反应:2X(g)+Y(g)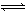 Z(g)+W(s) ΔH>0,下列叙述正确的是
Z(g)+W(s) ΔH>0,下列叙述正确的是
| A.在容器中加入氩气,反应速率不变 |
| B.加入少量W,逆反应速率增大 |
| C.升高温度,正反应速率增大,逆反应速率减小 |
| D.将容器的体积压缩,可增大单位体积内活化分子的百分数,有效碰撞次数增大 |
用CO合成甲醇(CH3OH)的化学反应方程式为CO(g)+2H2(g) CH3OH(g) △H<0
CH3OH(g) △H<0
按照相同的物质的量投料,测的CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )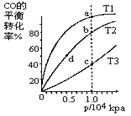
| A.平衡常数:K(a)>K(c) K(b)=K(d) |
| B.正反应速率:v(a)>v(c) v(b)>v(d) |
| C.平均摩尔质量:M(a)<M(c) M(b)>M(d) |
| D.平衡时a点一定有n(CO):n(H2)=1:2 |
已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H="74.9" kJ·mol-1,下列说法中正确的是
| A.该反应中熵变、焓变皆大于0 |
| B.该反应是吸热反应,因此一定不能自发进行 |
| C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行 |
| D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
一定温度下,在2L密闭容器中发生下列反应:4NO2(g)+O2(g) 2N2O5(g);已知该反应的平衡常数:
2N2O5(g);已知该反应的平衡常数: >
> ,且体系中
,且体系中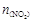 (单位:mol)随时间变化如下表:
(单位:mol)随时间变化如下表:
| 时间(s) | 0 | 500 | 1000 | 1500 |
| t1℃ | 20 | 13.96 | 10.08 | 10.08 |
| t2℃ | 20 | a | b | c |
下列说法一定正确的是( )
A.正反应为吸热反应
B.如果t2℃<t1℃,那么 a>b=c,且a=10+0.5b
C.如果t2℃<t1℃,那么t2℃达到平衡的时间介于1000s至1500s之间
D.如果t2℃>t1℃,那么b>10.08
下列叙述中,不能用平衡移动原理解释的是
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.黄绿色的氯水光照后颜色变浅 |
| C.由H2、Br2(g)、HBr(g)气体组成的平衡体系加压后颜色变深 |
| D.工业合成氨反应中加压有利于提高氨气的产率 |
在一定温度下,向容积固定不变的密闭容器中充入amolNO2,发生如下反应:
2NO2(g) N2O4(g);△H<0。达平衡后再向容器中充入amolNO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
N2O4(g);△H<0。达平衡后再向容器中充入amolNO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
| A.平均相对分子质量增大 | B.NO2的转化率提高 |
| C.NO2的质量分数增大 | D.反应放出的总热量大于原来的2倍 |