题目内容
下列各组中的两种物质相互反应时,无论哪种过量,都可以用同一个离子方程式表示的是( )
①碳酸钠溶液与盐酸②偏铝酸钠溶液与盐酸③氯化铝溶液与氨水 ④硫酸氢钠与氢氧化钡.
①碳酸钠溶液与盐酸②偏铝酸钠溶液与盐酸③氯化铝溶液与氨水 ④硫酸氢钠与氢氧化钡.
| A、③⑤ | B、①③ | C、仅有③ | D、②④ |
考点:离子方程式的书写
专题:离子反应专题
分析:①碳酸钠与少量盐酸:Na2CO3+HCl=NaHCO3+NaCl;与过量盐酸反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
②偏铝酸钠溶液与少量盐酸:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl;偏铝酸钠溶液与过量盐酸:NaAlO2+4HCl=AlCl3+2H2O↑;
③氯化铝溶液与氨水:AlCl3+3NH3.H2O=Al(OH)3↓+3NH4Cl;
④硫酸氢钠与少量氢氧化钡:2 NaHSO4+Ba(OH)2=BaSO4↓+2H2O+Na2SO4;硫酸氢钠与过量氢氧化钡:NaHSO4+Ba(OH)2 =BaSO4↓+NaOH+H2O.
②偏铝酸钠溶液与少量盐酸:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl;偏铝酸钠溶液与过量盐酸:NaAlO2+4HCl=AlCl3+2H2O↑;
③氯化铝溶液与氨水:AlCl3+3NH3.H2O=Al(OH)3↓+3NH4Cl;
④硫酸氢钠与少量氢氧化钡:2 NaHSO4+Ba(OH)2=BaSO4↓+2H2O+Na2SO4;硫酸氢钠与过量氢氧化钡:NaHSO4+Ba(OH)2 =BaSO4↓+NaOH+H2O.
解答:
解:①碳酸钠溶液与盐酸,反应物用量不同,发生反应不同,离子方程式不同,故①错误;
②偏铝酸钠溶液与盐酸,反应物用量不同,发生反应不同,离子方程式不同,故②错误;
③氯化铝溶液与氨水,反应与反应物的用量无关,离子方程式相同,均为AlCl3+3NH3.H2O=Al(OH)3↓+3NH4Cl,故③正确;
④硫酸氢钠与氢氧化钡,反应物用量不同,发生反应不同,离子方程式不同,故④错误;
故选C.
②偏铝酸钠溶液与盐酸,反应物用量不同,发生反应不同,离子方程式不同,故②错误;
③氯化铝溶液与氨水,反应与反应物的用量无关,离子方程式相同,均为AlCl3+3NH3.H2O=Al(OH)3↓+3NH4Cl,故③正确;
④硫酸氢钠与氢氧化钡,反应物用量不同,发生反应不同,离子方程式不同,故④错误;
故选C.
点评:本题考查离子方程式的书写,明确物质的性质是解本题关键,注意有些离子反应方程式与反应物的量有关,题目难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
下列各组离子在相应的条件下可能大量共存的是( )
| A、能使pH试纸变红的溶液中:CO32-、Ba2+、Cl-、Na+ | ||
| B、由水电离产生的c(OH-)=1×10-10 mol/L的溶液中:NO3-、Mg2+、SO42-、Fe2+ | ||
C、在
| ||
| D、无色透明溶液中:Al3+、HCO3-、Cl-、K+ |
下列各物质的溶液物质的量浓度均为0.1mol/L:①HCl;②NaOH;③Na2CO3;④NH4Cl;⑤CH3COONa;⑥Ba(OH)2;⑦KCl.它们pH按由小到大的排列顺序为( )
| A、⑥②③⑤⑦④① |
| B、①④⑦③⑤②⑥ |
| C、①④⑤③⑦②⑥ |
| D、①④⑦⑤③②⑥ |
英国物理学家约翰?丁达尔首先发现了入射光透过胶体时,从侧面可以看到一条光亮的通路.下列液体中,不会出现丁达尔效应的分散系的是( )①鸡蛋白溶液 ②肥皂水 ③淀粉溶液 ④硝酸钾溶液.
| A、① | B、② | C、④ | D、③ |
在相同条件下,下列气体中密度最大的是( )
| A、H2 |
| B、O2 |
| C、C12 |
| D、HCl |
第一次用无机物制备有机物尿素,开辟人工合成有机物先河的科学家是( )
| A、德国的维勒 |
| B、英国的道尔顿 |
| C、德国的李比希 |
| D、俄罗斯的门捷列夫 |
下列有关金属和金属材料的说法错误的是( )
| A、铁有良好的导热性,常用来制作炊具 |
| B、铜的化学性质不活泼,在潮湿的空气中不会生锈 |
| C、废旧电池中汞的回收可减少对环境的污染 |
| D、铝表面易形成致密的氧化膜可阻止铝进一步被氧化 |
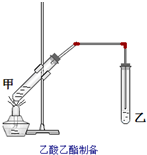 如图在试管甲中先加入2mL乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:
如图在试管甲中先加入2mL乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答: