题目内容
9.物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种.请根据所学化学知识回答下列问题:(1)A为0.1mol/L的(NH4)2SO4溶液,在该溶液中离子浓度由大到小的顺序为c(NH4+)>c(SO42-)>c(H+)>c(OH-).
(2)B为0.1mol/L的NaHCO3溶液,NaHCO3在该溶液中存在的平衡有(用离子方程式表示)HCO3-?H++CO32-、HCO3-+H2O?H2CO3+OH-.
(3)C为0.1mol/L的(NH4)2Fe(SO4)2溶液,与同浓度的(NH4)2SO4溶液中相比较(NH4)2Fe(SO4)2(填溶质的化学式)溶液中NH${\;}_{4}^{+}$的浓度更大,其原因是;NH4+和Fe2+都水解呈酸性,水解相互抑制.
(4)D为含有足量AgCl固体的饱和溶液,AgCl在溶液中存在如下平衡:
AgCl(s)???Ag+(aq)+Cl-(aq)
在25℃时,AgCl的Ksp=1.8×10-10.现将足量AgCl固体分别放入下列液体中:
①100mL蒸馏水 ②100mL 0.3mol/LAgNO3溶液 ③100mL 0.1mol/LMgCl2
溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为②①③(填序号),此时溶液②中Cl-物质的量浓度为6×10-10mol/L.
分析 (1)硫酸铵为强酸弱碱盐,铵根离子水解导致溶液呈酸性,再结合电荷守恒判断离子浓度大小;
(2)碳酸氢钠溶液中存在碳酸氢根离子的水解、电离平衡;
(3)亚铁离子和铵根水解均显酸性,亚铁离子水解抑制铵根的水解,(NH4)2Fe(SO4)2溶液中c(NH4+)稍大,以此解答该题;
(4)含有银离子或氯离子的溶液抑制AgCl溶解,氯离子或银离子浓度越大其抑制AgCl溶解程度越大.
解答 解:(1)硫酸铵为强酸弱碱盐,铵根离子水解导致溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒得c (NH4+)>c(SO42-),铵根离子水解程度较小,则溶液中离子浓度大小顺序是c(NH4+)>c(SO42-)>c(H+)>c(OH-),
故答案为:c(NH4+)>c(SO42-)>c(H+)>c(OH-);
(2)碳酸氢钠溶液中存在碳酸氢根离子的水解、电离平衡,其离子方程式分别为:HCO3-?H++CO32-、HCO3-+H2O?H2CO3+OH-,
故答案为:HCO3-?H++CO32-、HCO3-+H2O?H2CO3+OH-;
(3)(NH4)2Fe(SO4)2中NH4+和Fe2+都水解呈酸性,水解相互抑制,因此(NH4)2Fe(SO4)2中NH4+的水解程度(NH4)2SO4的要小,(NH4)2Fe(SO4)2比(NH4)2SO4的c(NH4+)大.
故答案为:(NH4)2Fe(SO4)2;NH4+和Fe2+都水解呈酸性,水解相互抑制;
(4)含有银离子或氯离子的溶液抑制AgCl溶解,氯离子或银离子浓度越大其抑制AgCl溶解程度越大,氯化镁和硝酸银溶液抑制AgCl溶解,但硝酸银是可溶性盐,所以硝酸银溶液中银离子浓度最大,则Ag+浓度由大到小的顺序为②①③,c(Cl-)=$\frac{1.8×1{0}^{-10}}{0.3}$mol/L=6×10-10 mol/L,
故答案为:②①③;6×10-10 mol/L.
点评 本题考查了离子浓度大小比较、难溶物的溶解平衡等知识点,根据溶质的性质结合电荷守恒判断离子浓度大小,根据溶度积常数计算氯离子浓度,题目难度不大.

 名校通行证有效作业系列答案
名校通行证有效作业系列答案| A. | 将2-氯丙烷与NaOH的醇溶液共热制备CH3-CH═CH2 | |
| B. |  与适量NaOH溶液反应制备 与适量NaOH溶液反应制备 | |
| C. | 用分液法分离苯和液溴的混合物 | |
| D. | 向卤代烃水解后的溶液中直接加入硝酸银溶液,可以确定卤代烃中的卤元素 |
 氨在工农业生产中应用广泛.在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如图:
氨在工农业生产中应用广泛.在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如图:| 温度/℃ | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
(1)根据如图,合成氨的热化学方程式是N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ•mol-1.
(2)取1mol N2(g)和3mol H2(g)放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量小于92.2kJ(填“大于”“等于”或“小于”),原因是该反应是可逆反应,反应物无法全部转化为生成物;若加入催化剂,△H不变(填“变大”“变小”或“不变”).
(3)已知:分别破坏1mol N≡N键、1mol H-H键需要吸收的能量为:946kJ、436kJ,则破坏1mol N-H键需要吸收的能量为391kJ.
(4)N2H4可视为:NH3分子中的H被-NH2取代的产物.发射卫星用N2H4(g)为燃料,NO2为氧化剂生成N2和H2O(g).
已知:N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJ•mol-1
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H2=-534kJ•mol-1.
则:1mol N2H4与NO2完全反应的热化学方程式为N2H4(g)+NO2(g)═$\frac{3}{2}$N2(g)+2H2O(g)△H=-567.85kJ•mol-1.
(已知某温度下2HI(g)?H2(g)+I2(g)△H=+AkJ•mol-1 K=4.0)
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2 mol HI | 1mol H2+1mol I2 | 2mol HI+1mol H2+1mol I2 |
| HI的浓度 | c1 | c2 | c3 |
| 反应的能量变化 | 吸收akJ | 放出bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
①c1、c3的关系式为2c1=c3
②a、b的关系式为a+b=A
③p2、p3的关系式为2p2=p3
④a1与a2的关系式为α1+α2=1
(2)甲容器中:该反应的平衡常数表达式为K=$\frac{c({H}_{2})•c({I}_{2})}{{c}^{2}(HI)}$.
(3)乙容器中:反应在开始2分钟后达平衡状态,则该反应在这2分钟内用HI表示的平均反应速率为0.1mol•L-1•min-1
(4)丙容器中:反应开始时V正大于V逆(填“小于”、“等于”或“大于”)
| A. | 在4mL0.1mol/L的K2Cr2O7溶液中滴加数滴1mol/LNaOH溶液,溶液颜色从橙色变成黄色 | |
| B. | 向血红色的Fe(SCN)3溶液中加入少量KI固体,溶液颜色变浅 | |
| C. | 在试管中加入少量氯化钴晶体,滴加浓盐酸溶解后加水稀释至紫色,将试管置于热水中片刻,溶液颜色变成粉红色 | |
| D. | 用50mL针筒抽取30mL红棕色的NO2气体并封住注射孔,当用力推压活塞,压缩针筒中的气体(此过程中不考虑温度变化),从针筒顶端观察,气体颜色逐渐变浅 |
| A. | 1000mL水中所含K+、SO42-总数为0.15NA | |
| B. | 500mL溶液中含有0.1NA个K+ | |
| C. | 1L溶液中K+的浓度为0.1mol/L | |
| D. | 1L溶液中SO42-的浓度是0.2mol/L |
| A. | 75.77%表示35Cl的质量分数 | |
| B. | 35.5表示氯元素的近似相对原子质量 | |
| C. | 24.23%表示35Cl的丰度 | |
| D. | 36.966表示37Cl的质量数 |
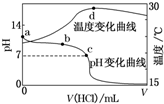 室温下,将1.000mol•L-1盐酸滴入20.00mL1.000mol•L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将1.000mol•L-1盐酸滴入20.00mL1.000mol•L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )| A. | a点由水电离出的c(H+)=1.0×10-14 mol•L-1 | |
| B. | b点:c(NH${\;}_{4}^{+}$)+c(NH3•H2O)=c(Cl-) | |
| C. | c点:c(Cl-)=c(NH${\;}_{4}^{+}$) | |
| D. | d点后,溶液温度略下降的主要原因是NH3•H2O电离吸热 |