题目内容
18. 室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室.分别向A、B两室充入H2、O2的混合气体和1mo1空气.此时活塞的位置如图所示.
室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室.分别向A、B两室充入H2、O2的混合气体和1mo1空气.此时活塞的位置如图所示.(1)A室混合气体的物质的量为2mol,所含分子总数为1.204×1024;
(2)实验测得A室混合气体的质量为34g,则该混合气体的密度是同温同压条件下氦气密度的8.5倍,该混合气体中H2和O2的物质的量之比为1:1.
分析 (1)同温同压下,气体的物质的量之比等于其气体之比;根据N=nNA计算分子数目;
(2)计算A室中混合气体的平均摩尔质量,同温同压下气体的密度之比等于其摩尔质量之比;
根据总质量、总物质的量列方程计算氢气与氧气物质的量.
解答 解:(1)A、B两室压强与温度相同,气体的物质的量之比等于其气体之比,则A室中气体物质的量为1mol×$\frac{4}{2}$=2mol,含有分子数目为2mol×6.02×1023mol-1=1.204×1024,
故答案为:2mol;1.204×1024;
(2)A室中混合气体的平均摩尔质量为$\frac{34g}{2mol}$=17g/mol,同温同压下气体的密度之比等于其摩尔质量之比,故该混合气体的密度是同温同压条件下氦气密度$\frac{17}{2}$=8.5倍,
设氢气物质的量为xmol、氧气物质的量为ymol,则:
$\left\{\begin{array}{l}{x+y=2}\\{2x+32y=34}\end{array}\right.$
解得x=1、y=1,
则H2与O2的物质的量之比为1mol:1mol=1:1,
故答案为:8.5;1:1.
点评 本题考查阿伏伽德罗定律及其推论,侧重考查学生计算能力,注意根据PV=nRT理解阿伏伽德罗定律及其推论.

练习册系列答案
相关题目
4.下列说法错误的是( )
| A. | 由单质A转化为单质B,△H=+119kJ/mol,可知单质A比单质B稳定 | |
| B. | 灼热的碳与CO2反应既是氧化还原反应,又是吸热反应 | |
| C. | 决定化学反应速率的根本因素是参加反应的各物质的结构和性质 | |
| D. | 对于一个可逆反应(△H<0)达到平衡后,升高温度可以使V正增大的倍数大于V逆增大的倍数,从而使化学反应平衡逆向移动 |
6.已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法.
Ⅰ.还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬.
具体流程如下:

有关离子完全沉淀的pH如下表:
(1)写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O.
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.亚硫酸氢钠 C.生石灰 D.铁屑
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.
则在操作②中可用于调节溶液pH的试剂为:CD(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
Ⅱ.电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-.
(5)电解法中加入氯化钠的作用是:增强溶液导电性.
Ⅰ.还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬.
具体流程如下:

有关离子完全沉淀的pH如下表:
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.亚硫酸氢钠 C.生石灰 D.铁屑
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.
则在操作②中可用于调节溶液pH的试剂为:CD(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
Ⅱ.电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-.
(5)电解法中加入氯化钠的作用是:增强溶液导电性.
10.将一小块金属钠投入下列物质的溶液中,既能放出气体,又有沉淀析出的是( )
| A. | NH4Cl | B. | BaCl2 | C. | CuCl2 | D. | NaHCO3 |
7.下列操作或仪器选用不正确的是( )
| A. | 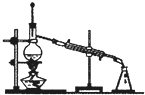 石油蒸馏 | B. |  检验Fe3+ | C. |  制备氨气 | D. |  中和滴定 |
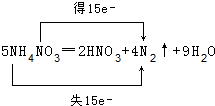

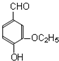 )是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称:酚羟基、醛基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
)是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称:酚羟基、醛基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
 ,属于取代反应(填反应类型).
,属于取代反应(填反应类型). .
. .
. )是一种医药中间体,请设计合理方案用茴香醛(
)是一种医药中间体,请设计合理方案用茴香醛( )合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
)合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
 .
.