题目内容
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。工业设计生产NaClO2的主要流程如下:
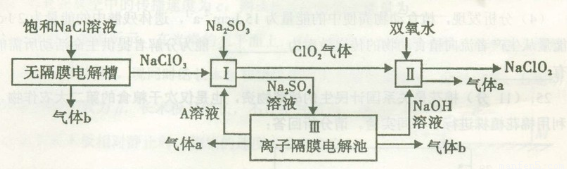
(1)A的化学式是???????? ,装置III中A在???????? 极区产生。
(2)II中反应的离子方程式是???????????????? 。
(3)通电电解前,检验III中阴离子的方法和步骤是????????????????? 。
(4)为防止II中制备的NaClO2被还原成NaCl,应选合适的还原剂,除双氧水外,还可以选择的还原剂是 ?????? (填字母编号)。
a.Na2O2 ???? ? b.FeCl2?? ??? c.Na2S
(5)常温时,HClO2的电离平衡常数Ka=1.07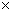 10-2mol·L-1,II中反应所得NaClO2溶液(含少量NaOH)的pH=13,则溶液中
10-2mol·L-1,II中反应所得NaClO2溶液(含少量NaOH)的pH=13,则溶液中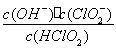 = ??????? 。
= ??????? 。
(6)气体a、b与氢氧化钠溶液可构成燃料电池,用该电池电解200 mL 0.5 mol·L-1的CuSO4溶液,生成铜3.2 g,此时所得溶液中离子浓度由大到小的顺序是 ??????????
(1)H2SO4? (2分)??? 阳(2分)
(2)2ClO2+H2O2+2OH-=2ClO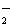 +O2↑+2H2O (3分)
+O2↑+2H2O (3分)
(3)取少量Ⅲ中溶液少许于试管中,先加入足量稀盐酸,无沉淀生成,再加入BaCl2溶
液,产生白色沉淀,证明含有SO42-? (3分)
(4)a(2分)
(5)1.07×1010mol·L-1 (3分)
(6)c(H+)>c(SO42-)>c(Cu2+)>c(OH-) (3分)
【解析】
试题分析:(1)Ⅲ为电解硫酸钠溶液,本质是电解水,阴极2H++2e-=H2↑,阳极4OH--4e-=O2↑+2H2O,另一电极产生NaOH,因为该电解池为离子隔膜电解池,所以A为硫酸,在阳极区产生。
(2))Ⅱ中反应根据流程信息可知,生成NaClO2,所以一定有ClO2→NaClO2,化合价降低,被还原;则H2O2必定被氧化,有氧气产生,反应中ClO2是氧化剂,发生还原反应,HCl是还原剂,发生氧化反应,根据电子转移守恒可知4n(ClO2)=n(HCl),所以反应方程式为:2NaOH+2ClO2+H2O2=2 NaClO2+2H2O+O2↑,离子方程式是2ClO2+H2O2+2OH-=2ClO2-+O2↑+2H2O。
(3)III中阴离子为SO42?,检验方法为:取少量Ⅲ中溶液少许于试管中,先加入足量稀盐酸,无沉淀生成,再加入BaCl2溶液,产生白色沉淀,证明含有SO42-
(4)加入FeCl2和Na2S会产生杂质,而Na2O2不会产生新的杂质,故a项正确。
(5)II中反应所得NaClO2溶液(含少量NaOH)的pH=13,可得c(H+)=1×10-13mol?L?1,则 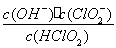 =
= =1.07×1010mol·L-1 。
=1.07×1010mol·L-1 。
(6)电解硫酸铜溶液的化学方程式为:2CuSO4+2H2O 2H2SO4+2Cu+O2↑,生成铜3.2 g,则反应了CuSO4的物质的量为0.05mol,生成H2SO4的物质的量为0.05mol,则所得溶液含0.05mol的CuSO4和0.05mol的H2SO4,Cu2+水解生成H+,所以离子浓度由大到小的顺序为:c(H+)>c(SO42-)>c(Cu2+)>c(OH-)。
2H2SO4+2Cu+O2↑,生成铜3.2 g,则反应了CuSO4的物质的量为0.05mol,生成H2SO4的物质的量为0.05mol,则所得溶液含0.05mol的CuSO4和0.05mol的H2SO4,Cu2+水解生成H+,所以离子浓度由大到小的顺序为:c(H+)>c(SO42-)>c(Cu2+)>c(OH-)。
考点:本题考查化学工艺流程的分析、电解原理、离子方程式的书写、离子的检验、化学计算。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(10分)氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:
Cl2 + H2O  HCl + HClO K=4.5×10-4
HCl + HClO K=4.5×10-4
次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其它性能优越的消毒产品所替代。请回答:
(1)氯碱工业生产氯气的化学方程式为 。
(2)84消毒液(主要成分为NaClO)与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为 。
(3)二氧化氯是一种高效、广谱、安全的杀菌、保鲜剂。我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为 。
(4)一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧
化性强弱的微型装置(如图)。
①下列溶液能吸收Cl2的是 (填字母序号)。
| A.饱和食盐水 | B.饱和Na2SO3溶液 |
| C.饱和NaOH溶液 | D.浓硫酸 |
(10分)氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:
Cl2 + H2O
 HCl
+ HClO K=4.5×10-4
HCl
+ HClO K=4.5×10-4
次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其它性能优越的消毒产品所替代。请回答:
(1)氯碱工业生产氯气的化学方程式为 。
(2)84消毒液(主要成分为NaClO)与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为 。
(3)二氧化氯是一种高效、广谱、安全的杀菌、保鲜剂。我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为 。
(4)一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧
化性强弱的微型装置(如图)。

①下列溶液能吸收Cl2的是 (填字母序号)。
A. 饱和食盐水 B. 饱和Na2SO3溶液
C. 饱和NaOH溶液 D. 浓硫酸
②能说明Cl2的氧化性强于I2的实验现象是 。
 (2013?江西模拟)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、
(2013?江西模拟)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、