题目内容
4.香豆素类化合物具有抗病毒、抗癌等多种生活活性,香豆素-3-羧酸可由水杨醛制备.下列说法正确的是( )
| A. | 水杨醛分子中有三种官能团 | |
| B. | 中间体X易溶于水 | |
| C. | 香豆素-3-羧酸能使酸性高锰酸钾溶液褪色 | |
| D. | l mol水杨醛最多能与3 molH2发生加成反应 |
分析 A.水杨醛含-OH、-CHO;
B.中间体X属于酯类物质,难溶于水;
C.香豆素-3-羧酸含有碳碳双键,能使酸性高锰酸钾溶液褪色;
D.苯环和醛基都可与氢气发生加成反应.
解答 解:A.水杨醛含-OH、-CHO,有2种官能团,故A错误;
B.中间体X属于酯类物质,难溶于水,故B错误;
C.香豆素-3-羧酸含有碳碳双键,可与酸性高锰酸钾发生氧化还原反应,故C正确;
D.苯环和醛基都可与氢气发生加成反应,则lmol水杨醛最多能与4 molH2发生加成反应,故D错误.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意烯烃、醛的性质,题目难度不大.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
14.下列说法正确的是( )
| A. | KAl(SO4)2 溶液中 c(K+)=2c(SO42-) | |
| B. | 向NaHCO3溶液中加入少量Ba(OH)2固体,c(CO32-)增大 | |
| C. | 含有A gCl 和A gBr 固体的悬浊液中,C(Ag+)>c(Cl-)=c(Br-) | |
| D. | 若使Na2S溶液中$\frac{{c(N{a^+})}}{{c({S^{2-}})}}$接近于2:1,可加入适量的NaOH固体 |
15.下列关于化学键的说法正确的是( )
| A. | 组成单质的分子内一定含有共价键 | |
| B. | 由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 测化合物在熔融或水溶液中的导电性可判断是否为离子化合物 | |
| D. | 化学反应中伴随的能量变化,所以反应一定会有热效应(即放热成吸热) |
12.下列关于晶体的说法一定正确的是( )


| A. | 分子晶体中都存在共价键 | |
| B. | 右图CaTiO3晶体中每个Ti4+与12个O2-相紧邻 | |
| C. | SiO2晶体中每个硅原子与两个氧原子以共价键相结合 | |
| D. | 在二氧化硅晶体中,最小环上的原子个数是六 |
9.固定容积为 2L 的密闭容器中发生反应 xA(g)+yB(g)?zC(g),图 I 表示 200℃时容器 中各物质的量随时间的变化关系,图 II 表示平衡时平衡常数 K 随温度变化的关系.结合图 像判断,下列结论正确的是( )


| A. | 200℃时,反应从开始到平衡的平均速率 v(A)=0.08 mol•L-1•min-1 | |
| B. | 若 0~5 min 时容器与外界的热交换总量为 m kJ,则该反应的热化学方程式可表示为:2A(g)+B(g)?C(g)△H=+5m kJ/mol | |
| C. | 200℃时,若在第 6 min 再向体系中加入催化剂,可使 v 正>v 逆 | |
| D. | 200℃时,平衡后再充入 2 mol C,则达到平衡时,化学平衡常数变小 |
16.下列叙述中正确的是( )
| A. | 两份质量相同的Al分别加入到足量NaOH溶液和盐酸中充分反应,盐酸增加的质量大 | |
| B. | 两份质量相同的S分别与足量NaOH溶液和Na反应,两者转移的电子数相同 | |
| C. | 相同物质的量的CO2、H2O分别与足量Na2O2反应,生成气体的物质的量相同 | |
| D. | H2分别通过灼热的CuO和Fe2O3粉末,当转移电子数相同时,Fe2O3减轻的质量大 |
13.实验室需用480mL 0.1mol/L的硫酸铜溶液,以下配制溶液操作正确的是.( )
| A. | 称取7.68g CuSO4,加入480mL水 | B. | 称取12.0g胆矾配成500 mL溶液 | ||
| C. | 称取8.0g CuSO4,加入500 mL水 | D. | 称取12.5g胆矾配成500 mL溶液 |
15.下列化学用语书写正确的是( )
| A. | 氯原子的结构示意图: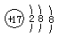 | |
| B. | CH4的球棍模型:? | |
| C. | 氯化镁的电子式: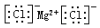 | |
| D. | 硫酸的电离方程式:H2SO4═H2++SO42ˉ |



 .
.