题目内容
15.下列物质性质与应用不存在对应关系的是( )| A. | K2FeO4具有强氧化性,可用作水处理剂 | |
| B. | 氢氧化铝具有弱碱性,可用作制胃酸中和剂 | |
| C. | 碳具有还原性,可用作锌锰干电池的正极材料 | |
| D. | 常温下浓硫酸能使铝发生钝化,可用铝制容器贮运浓硫酸 |
分析 A.K2FeO4具有强氧化性,可用于消毒杀菌,被还原为Fe3+,水解生成Fe(OH)3,具有吸附性;
B.氢氧化铝具有弱碱性,能中和酸;
C.原电池的正极不发生反应;
D.常温下,浓硫酸遇到铝发生钝化.
解答 解:A.K2FeO4具有强氧化性,可用于消毒杀菌,被还原为Fe3+,水解生成Fe(OH)3,具有吸附性,可用于吸附水中的悬浮杂质,所以高铁酸钾作水处理剂具有净水功能,故A正确;
B.胃酸的主要成分是HCl,氢氧化铝具有弱碱性,能中和酸,二者有对应关系,故B正确;
C.碳可用作锌锰干电池的正极材料,不参加电池反应,只起导体作用,所以与还原性无关,故C错误;
D.常温下,浓硫酸遇到铝发生钝化,形成在致密氧化膜,阻止反应进行,所以可用铝制容器贮运浓硫酸,故D正确;
故选:C.
点评 本题考查了物质间的关系,明确物质的性质是解本题关键,根据其性质分析用途,掌握物质的性质,灵活运用知识解答,注意原电池工作原理,题目难度不大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
5.下列卤代烃不能通过烯烃与相应卤化氢加成得到的是( )
| A. | CH3-CH2-Br | B. | 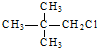 | ||
| C. | 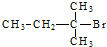 | D. | 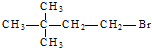 |
6.下列过程中,化学键一定被破坏的是( )
| A. | 碘升华 | B. | 无色透明的水晶被粉碎 | ||
| C. | 蔗糖溶于水 | D. | HCl气体加压降温液化 |
3.下列说法错误的是( )
| A. | 硅胶疏松多孔,可用作催化剂的载体 | |
| B. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 | |
| C. | 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 | |
| D. | 氮的固定只有在高温、高压、催化剂的条件下才能实现 |
10.T℃时,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),发生反应:2SO2(g)+O2(g)?2SO3(g),5min时甲达到平衡.其起始量及SO2的平衡转化率如下表所示.下列叙述不正确的是( )
| 容器 | 甲 | 乙 | 丙 | |
| 起始量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率 | 80% | α1 | α2 | |
| A. | 0~5min内,甲中SO2的反应速率为0.032mol•L-1•min-1 | |
| B. | T℃时,该反应的平衡常数K=400 | |
| C. | 平衡时,甲、丙中气体密度分别为ρ1、ρ2,则ρ2>2ρ1 | |
| D. | 平衡时,SO2的转化率:α1<80%<α2 |
20.室温时,将xmLPH=a的稀盐酸与ymLPH=b的稀NaOH溶液充分反应,下列关于反应后溶液PH的判断正确的是( )
| A. | 若x=y,且a+b=14,则pH>7 | B. | 若10x=y,且a+b=13,则pH=7 | ||
| C. | 若ax=by,且a+b=14,则pH=7 | D. | 若x=10y,且a+b=14,则pH>7 |
5.下列对有机反应类型的认识中错误的是( )
| A. |  +HNO3$→_{△}^{浓硫酸}$ +HNO3$→_{△}^{浓硫酸}$  +H2O;取代反应 +H2O;取代反应 | |
| B. | CH2═CH2+Br2→CH2Br-CH2Br;加成反应 | |
| C. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;取代反应 | |
| D. | CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;酯化反应也属于取代反应 |
