题目内容
几种短周期元素的原子半径及主要化合价如下表:
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
已知X是短周期中最活泼的金属元素,且与R同周期。下列叙述不正确的是
A.离子半径大小:Y2- > M2- > R3+
B.Z与M组成的某种化合物能形成酸雨
C.Y与M组成的化合物跟水反应后一定能得强酸
D.X、Y、R的最高价氧化物的水化物两两之间能发生反应
C
【解析】
试题分析:根据化合价和原子半径的大小,X是短周期中最活泼的金属元素,且与R同周期可知,X为Na元素、Y为S元素、Z为N元素、M为O元素、R为Al元素。A、离子半径大小:S2? > O2? >Al3+,故A正确;B、Z与M可组成NO、NO2等,NO2能形成酸雨,故B正确;C、Y与M组成的化合物跟水反应可生成H2SO3或H2SO4,可能为强酸,也可能为弱酸,故C错误;D、X、Y、R的最高价氧化物的水化物分别为NaOH、H2SO4、Al(OH)3,因为Al(OH)3为两性氢氧化物,所以两两之间能发生反应,故D正确。
考点:本题考查元素的推断、原子结构。

练习册系列答案
相关题目
根据表中信息判断,下列选项不正确的是
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO4- | Cl2、Mn2+ |
A.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
B.第①组反应的氧化产物为O2
C.第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2
D.第③组反应中生成1mol Cl2,转移电子2mol
 的亚硫酸钠溶液,则在此反应中X元素的低价态为
的亚硫酸钠溶液,则在此反应中X元素的低价态为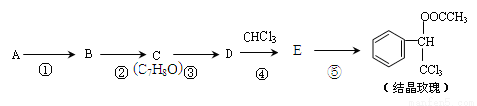
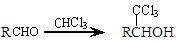 (-R表示烃基)
(-R表示烃基)