题目内容
常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L盐酸和20.00 mL 0.1000 mol/L醋酸溶液,得到2条滴定曲线,如下图所示:
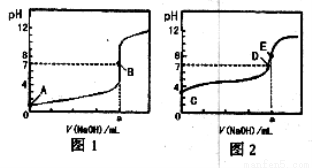
以HA表示酸,下列说法正确的是( )
A.滴定盐酸的曲线是图2
B.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A—)
C.达到B、E状态时,反应消耗的n( CH3COOH)>n(HCl)
D.当0mL< V(NaOH)<20.00mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)>c(Na+)>c(H+)>c(OH-)
B
【解析】
试题分析:A.由于盐酸是强酸,完全电离,醋酸是弱酸,部分电离,所以在酸浓度相同时,弱酸溶液的pH大,强酸的pH小,因此滴定盐酸的曲线是图1,错误;B.达到B、D状态时,溶液的pH=7,根据电荷守恒,即溶液呈电中性可得两溶液中离子浓度均为c(Na+)=c(A—),正确; C.达到B状态时,n(HCl)=n(NaOH);而达到E状态时,由于溶液显碱性,反应消耗的n( CH3COOH)可能等于n(NaOH),也可能小于或略多于n(NaOH),因此不能确定消耗的盐酸与醋酸的物质的量的多少,错误;D.由于图1是盐酸溶液的滴定曲线,当0mL< V(NaOH)<20.00mL时,盐酸过量,c(A-)>c(Na+);c(H+)>c(OH-);c(Na+)、c(H+)会随着滴定的NaOH的多少而发生改变,不一定谁大谁小,由大到小的顺序可能为c(A-)>c(Na+)>c(H+)>c(OH-),也可能是:c(A-)>c(H+)>c(Na+)>c(OH-),错误。
考点:考查强电解质、弱电解质的酸碱中和滴定、溶液中离子浓度的大小比较的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案几种短周期元素的原子半径及主要化合价如下表:
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
已知X是短周期中最活泼的金属元素,且与R同周期。下列叙述不正确的是
A.离子半径大小:Y2- > M2- > R3+
B.Z与M组成的某种化合物能形成酸雨
C.Y与M组成的化合物跟水反应后一定能得强酸
D.X、Y、R的最高价氧化物的水化物两两之间能发生反应
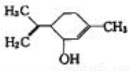
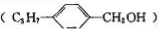 互为同分异构体
互为同分异构体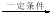 RCH=C(COOH)2+H2O,
RCH=C(COOH)2+H2O,