题目内容
6. 图是气体摩尔体积测定装置.
图是气体摩尔体积测定装置.(1)指出测定装置中仪器名称:a.储液瓶
使用该装置前必须作的第一步操作为检查装置气密性.
(2)为测定1mol氢气的体积,实验时,在气体发生器中,先加入称取除去表面氧化膜的镁带0.120g,用橡皮塞塞紧.用针筒(填仪器名称)在加料口将10.00mL稀硫酸加入气体发生器中,产生的氢气会把a中的液体压入b中,读出b中液体数据,转化成H2体积为129.250mL.
(3)若水蒸气的影响忽略不计,计算在该实验条件下的气体摩尔体积为25.85LVm.
分析 (1)依据图中仪器形状说出仪器的名称;依据实验目的,测定气体摩尔体积,可知该实验要求装置不能漏气;
(2)镁与稀硫酸反应生成氢气,用到的稀硫酸需要用针筒通过加料口进入气体发生器;
(3)依据Mg~H2,计算生成1mol氢气的体积Vm.
解答 解:(1)依据图中a仪器形状可知,其名称为储液瓶;依据实验目的,测定气体摩尔体积,可知该实验要求装置不能漏气,所以实验前应先检查是否漏水;
故答案为:储液瓶;
(2)镁与稀硫酸反应生成氢气,用到的稀硫酸需要用针筒通过加料口进入气体发生器;
故答案为:针筒;
(3)依据Mg~H2,设生成1mol氢气体积为Vm则;
24g Vm
0.120g 0.129250L
解得Vm=25.85L
故答案为:25.85L.
点评 本题考查了气体摩尔体积的测定,明确实验原理和装置特点即可解答,题目难度不大.

练习册系列答案
相关题目
11.将漂白粉配成溶液晾置在空气中,过了一段时间,其漂白效果会更好的原因可能是( )
| A. | 漂白粉被氧化了 | |
| B. | 有色布条被空气中的氧气氧化了 | |
| C. | 漂白粉跟空气中的 CO2反应充分,生成了较多量的 HClO | |
| D. | 漂白粉溶液蒸发掉部分水,其浓度增大 |
18.根据表中键能数据.计算反应HC1(g)=$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)的△H=+91.5kJ/mol.
| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能 | 436 | 243 | 431 |
15.如图是从元素周期表中截取下来的,A、B、C为短周期主族元素,下列说法中正确的是( )
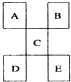

| A. | D一定足金属元素,其金属性比C强 | |
| B. | C的最高价氧化物水化物显强酸性 | |
| C. | E的原子序数一定是A的5倍,且原予半径比A大 | |
| D. | B的氢化物是以分子形式存在,且分子间存在氢键 |
16.下列第三周期的元素中,原子半径最小的是( )
| A. | S | B. | F | C. | Na | D. | O |
 如图是金属钨晶体中的一个晶胞的结构示意图,它是一种体心立方结构.实验测得金属钨的密度为19.30g•cm-3,钨的相对原子质量是183.9.假设金属钨原子为等径刚性球,试完成下列问题:
如图是金属钨晶体中的一个晶胞的结构示意图,它是一种体心立方结构.实验测得金属钨的密度为19.30g•cm-3,钨的相对原子质量是183.9.假设金属钨原子为等径刚性球,试完成下列问题: