题目内容
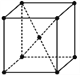
【题目】二氧化硅晶体是立体的网状结构,其晶体结构模型如图。请认真观察该模型后回答下列问题:
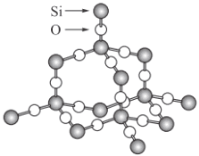
(1)二氧化硅晶体中最小环上有______个原子,晶体结构中存在以__________原子为中心、________原子为顶点的正四面体结构。
(2)晶体中存在的作用力有________。
A.共价键 B.离子键 C.配位键 D.范德华力 E.氢键
(3)美国LawreceLiremore国家实验室(LLNL)的V.Lota.C.S.Yoo和Cynn成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2的原子晶体说法正确的是________。
A.CO2的原子晶体和分子晶体互为同素异形体
B.在一定条件下,CO2原子晶体转化为分子晶体是物理变化
C.CO2的原子晶体和CO2的分子晶体具有相同的物理性质
D.在CO2的原子晶体中,每个C原子结合4个O原子,每个O原子结合两个C原子
【答案】12 Si O(或Si) A D
【解析】
(1)金刚石晶体中,最小的环为六元环,即由6个C原子构成,晶体硅的结构和金刚石相似,晶体硅的六元环也是由6个Si原子构成,可根据硅晶体中Si-Si之间插入O原子形成SiO2分析;结合给出的二氧化硅晶体结构模型找出符合正四面体结构的立体结构;
(2)二氧化硅为原子晶体;原子晶体中只存在共价键;
(3)A. 同素异形体为同种元素组成的不同的单质;
B. CO2原子晶体的结构类似二氧化硅晶体,CO2分子晶体则是彼此独立的二氧化碳分子之间以范德华力相互结合到一起的,两者转化时结构发生变化,二者是不同的物质;
C. CO2原子晶体和CO2分子晶体二者是不同的物质;
D. 根据二氧化硅的结构判断二氧化碳原子晶体的结构;据此分析。
(1) 金刚石晶体中,最小的环为六元环,即由6个C原子构成,晶体硅的结构和金刚石相似,晶体硅的六元环也是由6个Si原子构成,SiO2晶体可看作硅晶体中Si-Si之间插入O原子形成的,共插入六个O原子,则二氧化硅晶体中最小环上有6个硅原子和6个氧原子,共12个原子;并形成以硅原子为中心、氧原子(或硅原子)为顶点的正四面体结构;
故答案为:12;Si;O(或Si);
(2)原子晶体中只存在共价键,且Si—O键为极性键,不是配位键;
故答案为:A;
(3)A. 同素异形体的研究对象是单质,CO2是化合物,A项错误;
B. CO2的晶体类型发生转变已生成了新物质,且二者的性质也有较大差异,故二者是不同的物质,所以二者的转变是化学变化,B项错误;
C. CO2的原子晶体和CO2的分子晶体结构不同,二者是不同的物质,物理性质不同,C项错误;
D. CO2原子晶体类似于SiO2晶体,每个C原子结合4个O原子,每个O原子结合2个C原子,D项正确;
故答案为:D。