题目内容
13.反应 A+B→C(△H>0)分两步进行 ①A+B→X (△H<0)②X→C(△H>0),下列示意图中,能正确表示总反应过程中能量变化的是( )| A. | 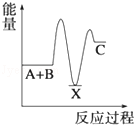 | B. | 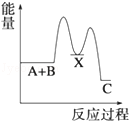 | C. |  | D. | 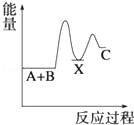 |
分析 根据物质具有的能量进行计算:△H=E(生成物的总能量)-E(反应物的总能量),当反应物的总能量大于生成物的总能量时,反应放热,当反应物的总能量小于生成物的总能量时,反应吸热,以此解答该题.
解答 解:由反应 A+B→C(△H>0)分两步进行:①A+B→X(△H<0),②X→C(△H>0),
由A+B→C(△H>0)是吸热反应,A和B的能量之和小于C;
由①A+B→X (△H<0)可知这步反应是放热反应,故X的能量小于A+B;
由②X→C(△H>0)可知这步反应是吸热反应,故X的能量小于C;
所以图象A符合,
故选A.
点评 本题依据图象主要考查了物质的能量分析应用,注意反应热与物质总能量大小的关系判断是解答本题的关键题目难度不大.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
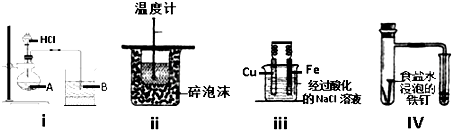
5.下列实验不能达到预期目的是( )
| A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| B | MgCl2、Al Cl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
| C | NaCO3溶液中加入稀H2SO4 | 比较碳、硫的非金属性强弱 |
| D | Fe、Cu分别与盐酸反应 | 比较铁、铜的金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
2.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,0.2NA个NH3分子的质量为3.4g | |
| B. | 2.7g金属铝所含电子数目为0.3NA | |
| C. | 7.1 g Cl2变为氯离子时,得到的电子数一定为0.1NA | |
| D. | 1L 0.2mol/L硫酸铁溶液中含有的SO42-离子数目为0.2NA |