题目内容
18.图是某种酶生物燃料电池的工作原理示意图.下列说法中不正确的是( )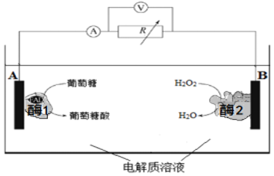
| A. | 葡萄糖是还原剂 | |
| B. | 外电路中电子由A极移向B极 | |
| C. | 溶液中H+ 由B极区移向A极区 | |
| D. | B极电极反应式为:H2O2+2H++2e-═2H2O |
分析 由图可知,葡萄糖失去电子转化为葡萄糖酸,过氧化氢得到电子生成水,则A为负极,B为正极,电子由负极流向正极,原电池中阳离子向正极移动,以此来解答.
解答 解:A.葡萄糖失去电子转化为葡萄糖酸,则葡萄糖为还原剂,故A正确;
B.A为负极,B为正极,电子由A极流向B极,故B正确;
C.B为正极,溶液中H+ 由A极区移向B极区,故C错误;
D.B极发生还原反应,电极反应式为:H2O2+2H++2e-═2H2O,故D正确;
故选C.
点评 本题考查化学电源,为高频考点,把握电极、电极反应为解答的关键,侧重分析与应用能力的考查,注意原电池的工作原理及应用,题目难度不大.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
4.工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.下列说法错误的是( )
| A. | 硫元素既被氧化,又被还原 | |
| B. | 氧化剂与还原剂的物质的量之比为2:1 | |
| C. | 相同条件下,每吸收10m3SO2就会放出2.5m3CO2 | |
| D. | 若生成2.24 L CO2,则转移0.8 mol电子 |
9.我国古代用炉甘石炼锌,主要反应为2C+ZnCO3 $\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑,该反应属于( )
| A. | 置换反应 | B. | 化合反应 | C. | 分解反应 | D. | 复分解反应 |
13.水中污染物不同,所采取的处理方法不同.下列处理方法不正确的是( )
| A. | 含Hg2+的废水--加入Na2S等沉淀剂 | |
| B. | 钢铁厂的酸性废水--加入熟石灰等进行中和 | |
| C. | 餐饮业厨房含油污水--加工为生物柴油进行利用 | |
| D. | 被细菌、病毒污染的饮用水--加入明矾等进行消毒 |
3.下列说法不正确的是( )
| A. | 石英是制造光导纤维的原料,也是常用的半导体材料 | |
| B. | 氧化铝是冶炼金属铝的原料,也是较好的耐火材料 | |
| C. | 与铜质水龙头的钢质水管,在连接处易发生腐蚀 | |
| D. | 大量燃烧化石燃料是造成雾霾的重要因素之一 |
10.已知:①H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/mol
②H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ/mol
下列说法不正确的是( )
②H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ/mol
| 气态分子中的化学键 | 断开1mol化学键所需的能量/kJ |
| O-H | 463 |
| O=O | 498 |
| A. | 氢气的燃烧热是△H=-241.8 kJ/mol | |
| B. | 断开1mol H-H键需要吸收435.2 kJ的能量 | |
| C. | 相同条件下,1 molH2O(g)比1 mol H2O(l)能量高 | |
| D. | 18 g H2O(l)完全分解生成氢气和氧气,需要吸收285.8 kJ的能量 |
7.香兰素是重要的香料之一,它可由丁香酚经多步反应合成.
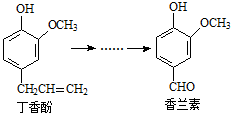
有关上述两种化合物的说法错误的是( )

有关上述两种化合物的说法错误的是( )
| A. | 丁香酚与香兰素都能与H2发生加成反应 | |
| B. | 常温下,1 mol丁香酚最多消耗1 mol Br2 | |
| C. | 丁香酚和香兰素遇FeCl3溶液都能发生显色反应 | |
| D. | 常温下,丁香酚与香兰素都能与浓溴水发生反应 |
