题目内容
4.工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.下列说法错误的是( )| A. | 硫元素既被氧化,又被还原 | |
| B. | 氧化剂与还原剂的物质的量之比为2:1 | |
| C. | 相同条件下,每吸收10m3SO2就会放出2.5m3CO2 | |
| D. | 若生成2.24 L CO2,则转移0.8 mol电子 |
分析 工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2,其反应方程式为2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2,反应在S元素的化合价从-2价升高到+2价,S的化合价从+4价降低到+2价,据此分析.
解答 解:A.由反应方程式中S元素的化合价变化可知,硫元素既被氧化又被还原,故A正确;
B.2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2中,Na2S为还原剂,SO2为氧化剂,则氧化剂与还原剂的物质的量之比为2:1,故B正确;
C.根据方程式可知,每当4molSO2参与氧化还原反应就会放出1molCO2,则每10m3SO2参与反应就会放出2.5m3CO2,由于二氧化碳溶于水,所以产生的二氧化碳少于2.5m3,故C正确;
D.状况不知无法由体积求物质的量,故D错误.
故选D.
点评 本题考查了氧化还原反应,注意根据反应物和生成物写出反应方程式,结合元素化合价的变化分析,题目难度中等.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
14.下列离子方程式书写正确的是( )
| A. | 铝粉投入氢氧化钠溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| B. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | |
| C. | 澄清石灰水跟稀硝酸反应:OH-+H+═H2O | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
15.下列离子方程式正确的是( )
| A. | 向氨水通入足量SO2:SO2+2NH3•H2O═2NH4++SO32-+H2O | |
| B. | 将Ba(OH)2溶液滴入NaHSO4溶液中至SO42-恰好完全沉淀:Ba2++SO42-+2OH-+2H+═BaSO4↓+2H20 | |
| C. | 向醋酸溶液中滴加过量NaOH溶液:H++OH-═H2O | |
| D. | 向新制Cu(OH)2悬浊液中加入乙醛溶液并加热:CH3CHO+2Cu(OH)2+OH-$\stackrel{加热}{→}$ CH3COO-+Cu2O↓+3H2O |
19.下列反应可用离子方程式“H++OH-=H2O”表示的是( )
| A. | NaHSO4溶液与Ba(OH)2溶液混合 | B. | 氢氧化镁溶于盐酸 | ||
| C. | 澄清石灰水与硝酸混合 | D. | 醋酸除去水垢 |
9.下列实验能达到实验目的是( )
| A. | 将CuCl2溶液小心蒸干得到无水CuCl2 | |
| B. | 用AgNO3溶液鉴别NO2和Br2蒸气 | |
| C. | 电解熔融的AlCl3制备金属铝 | |
| D. | 用饱和Na2CO3溶液除去CO2气体中混有的HCl |
17.关于如图所示两个装置的叙述中不正确的是( )
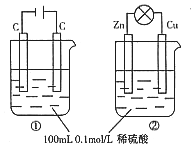

| A. | c(H+)浓度变化:①减小,②减小 | |
| B. | 装置名称:①是电解池,②是原电池 | |
| C. | 离子移动方向:①中H+向阴极方向移动,②中H+向正极方向移动 | |
| D. | 电极反应式:①中阳极:2H2O-4e-=4H++O2↑,②中负极:Zn-2e-=Zn2+ |
18.图是某种酶生物燃料电池的工作原理示意图.下列说法中不正确的是( )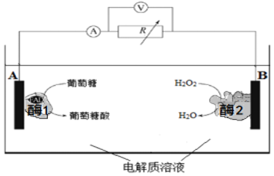

| A. | 葡萄糖是还原剂 | |
| B. | 外电路中电子由A极移向B极 | |
| C. | 溶液中H+ 由B极区移向A极区 | |
| D. | B极电极反应式为:H2O2+2H++2e-═2H2O |
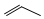
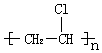 的单体是CH2=CHCl.
的单体是CH2=CHCl.