题目内容
3.下列说法不正确的是( )| A. | 石英是制造光导纤维的原料,也是常用的半导体材料 | |
| B. | 氧化铝是冶炼金属铝的原料,也是较好的耐火材料 | |
| C. | 与铜质水龙头的钢质水管,在连接处易发生腐蚀 | |
| D. | 大量燃烧化石燃料是造成雾霾的重要因素之一 |
分析 A.石英对光具有良好的全反射作用,不具有金属性和非金属性,不能作半导体材料;
B.氧化铝的熔点高,为离子化合物;
C.与铜质水龙头的钢质水管,构成原电池时Fe为负极;
D.大量燃烧化石燃料,排放大量固体颗粒物.
解答 解:A.石英对光具有良好的全反射作用,石英是制造光导纤维的原料,而Si是常用的半导体材料,故A错误;
B.氧化铝的熔点高,是较好的耐火材料,为离子化合物,可电解冶炼Al,故B正确;
C.与铜质水龙头的钢质水管,构成原电池时Fe为负极,则在连接处易发生腐蚀,故C正确;
D.大量燃烧化石燃料,排放大量固体颗粒物,则是造成雾霾的重要因素之一,故D正确;
故选A.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、性质与用途为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
9.下列实验能达到实验目的是( )
| A. | 将CuCl2溶液小心蒸干得到无水CuCl2 | |
| B. | 用AgNO3溶液鉴别NO2和Br2蒸气 | |
| C. | 电解熔融的AlCl3制备金属铝 | |
| D. | 用饱和Na2CO3溶液除去CO2气体中混有的HCl |
14.下列实验方法正确的是( )
| A. | 用分液漏斗分离乙酸和乙酸乙酯 | |
| B. | 用酚酞浓液鉴别未知浓度的NaOH溶液和Na2CO3溶液 | |
| C. | 用品红溶液鉴別SO2和CO2两种气体 | |
| D. | 用Ca(OH)2溶液鉴別Na2CO3 溶液和Na2HCO3溶液 |
11.某无土栽培的营养液按表要求配制.
(1)写出K2SO4的电离方程式K2SO4═2K++SO42-.
(2)若配制该营养液,取74.5gKCl,则需NH4Cl的质量是428.0g.
(3)配制过程如图乙所示,则图甲操作应在图乙中的③和④(填数字序号)之间;操作③的名称是转移溶液,其中玻璃棒下端的位置在容量瓶刻度线的下方.

| 营养液的成分 | KCl、K2SO4、NH4Cl |
| 物质的量之比 | n(KCl):n(K2SO4):n(NH4Cl)=1:4:8 |
(2)若配制该营养液,取74.5gKCl,则需NH4Cl的质量是428.0g.
(3)配制过程如图乙所示,则图甲操作应在图乙中的③和④(填数字序号)之间;操作③的名称是转移溶液,其中玻璃棒下端的位置在容量瓶刻度线的下方.

18.图是某种酶生物燃料电池的工作原理示意图.下列说法中不正确的是( )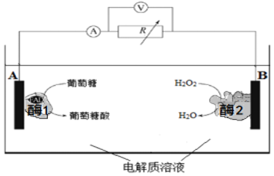

| A. | 葡萄糖是还原剂 | |
| B. | 外电路中电子由A极移向B极 | |
| C. | 溶液中H+ 由B极区移向A极区 | |
| D. | B极电极反应式为:H2O2+2H++2e-═2H2O |
8.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol甲醇分子中含有的共价键数为4 NA | |
| B. | 7.8g Na2O2固体与水完全反应时,转移的电子数为0.1NA | |
| C. | 标准状况下,11.2 L水中含有的氧原子数为0.5 NA | |
| D. | 1 L 0.5 mol/L CH3COONa溶液中含有的CH3COO-数为0.5 NA |
12.硅及其化合物在材料领域中应用广泛.下列叙述正确的是( )
| A. | 晶体硅可做光导纤维 | B. | SiO2可做计算机芯片 | ||
| C. | SiO2可与水反应制备硅胶 | D. | 玻璃、水泥、陶瓷都是硅酸盐产品 |
13.下列说法不正确的是( )
| A. | 与Na反应时,乙醇的反应速率比水慢 | |
| B. | 除去乙烷中混有的少量乙烯的方法是通入溴水 | |
| C. | 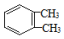 和 和 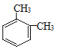 是同一种物质,说明苯分子中的碳碳键不是单双键交替的 是同一种物质,说明苯分子中的碳碳键不是单双键交替的 | |
| D. | 苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应 |
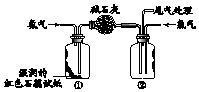 某同学利用图所示装置探究氨气的性质.
某同学利用图所示装置探究氨气的性质.