题目内容
6.某有机物A的结构简式为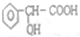
(1)请写出该有机物所含官能团的名称醇羟基和羧基.
(2)该物质能发生的反应类型有ABD(多项选择)
A.加成反应 B.氧化反应 C.加聚反应 D.取代反应 E.水解反应
(3)取一定量的A与足量金属钠反应,收集到气体体积为V1ml,另取等量的A与足量Na2CO3溶液反应,在相同状况下收集到气体体积为V2ml,V1、V2的等量代数关系式是:V1:V2=2:1.
(4)A物质在与浓硫酸共热时,能产生多种酯类化合物,其中当2个A分子之间脱去2个水分子后可以形成含有3个六元环的酯,写出该酯的结构简式:
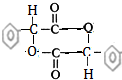 .
.
分析 (1)该物质中官能团是醇羟基和羧基;
(2)该物质中含有醇羟基、羧基和苯环,具有醇、羧酸和苯的性质;
(3)能和Na反应的有醇羟基和羧基,且醇羟基、羧基与Na反应的物质的量之比为1:1,生成的氢气物质的量与醇羟基或羧基的物质的量之比为1:2;只有羧基能和碳酸钠反应生成二氧化碳,且羧基与生成的二氧化碳物质的量之比为2:1;
(4)该物质中含有醇羟基和羧基,2分子的A之间发生酯化反应生成2分子水生成3个六元环的酯.
解答 解:(1)该物质中官能团是醇羟基和羧基,故答案为:醇羟基和羧基;
(2)该物质中含有醇羟基、羧基和苯环,具有醇、羧酸和苯的性质,醇羟基能发生氧化反应、取代反应、酯化反应,羧基能发生中和反应、取代反应、酯化反应,苯环能发生加成反应和取代反应,因为含有羧基和醇羟基而能发生缩聚反应,故选ABD;
(3)能和Na反应的有醇羟基和羧基,且醇羟基、羧基与Na反应的物质的量之比为1:1,生成的氢气物质的量与醇羟基或羧基的物质的量之比为1:2;只有羧基能和碳酸钠反应生成二氧化碳,且羧基与生成的二氧化碳物质的量之比为2:1,取等量的A分别和足量钠、碳酸钠反应生成氢气和二氧化碳的体积之比为2:1,即V1:V2=2:1,
故答案为:V1:V2=2:1;
(4)该物质中含有醇羟基和羧基,2分子的A之间发生酯化反应生成2分子水生成3个六元环的酯,其结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查学生分析推断及计算能力,注意羧基与足量碳酸钠或碳酸氢钠反应生成的二氧化碳的物质的量之比差别,题目难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
16.表给出了五种元素的相关信息,其中A、B、C、D为短周期元素.根据以下信息填空:
(1)C与A形成的气态化合物16g能和C与B形成的另一无色气态化合物(这两种化合物分子中原子个数比皆为1:2)发生反应生成无毒物质和液态水,并放出284kg的热量,写出上述热化学反应方程式:2 N2H4(g)+N2O4(g)=3N2(g)+4H2O(l)△H=-1136kJ/mol.
(2)化合物X是元素D的氢化物,X在水中的电离方程为H2S?H++HS-;元素E在元素周期表中的位置是第四周期第Ⅷ族.
| 元素 | 相关信息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 它在地壳中储量丰富,是人体不可缺少的微量元素之一.其单质为银白色固体,是工农业生产中不可或缺的金属材料,常用于机械制备、建筑等行业 |
(2)化合物X是元素D的氢化物,X在水中的电离方程为H2S?H++HS-;元素E在元素周期表中的位置是第四周期第Ⅷ族.
17.碱式碳酸铜的成分有多种,其化学式一般可表示为xCu(OH)2•yCuCO3.
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2•CuCO3.某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50mol•L-1的Cu(NO3)2溶液、2.0mL 0.50mol•L-1的NaOH溶液和0.25mol•L-1的Na2CO3溶液按表Ⅰ所示体积混合.
实验2:将合适比例的混合物在表Ⅱ所示温度下反应.
实验记录如下:
表Ⅰ表Ⅱ
①实验室制取少许孔雀石,应该采用的最佳条件是n[Cu(NO3)2]:n(Na2CO3)=2:1,75℃.
②80℃时,所制得的孔雀石有少量褐色物质的可能原因是Cu(OH)2受热分解为CuO.
(2)实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用如图所示的装置(夹持仪器省略)进行实验:
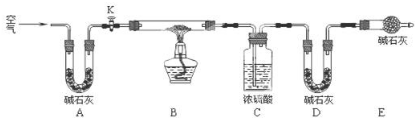
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中.
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量.
步骤3:加热装置B直至装置C中无气泡产生.
步骤4:(请补充该步操作内容).
步骤5:称量相关装置的质量.
①装置A的作用是;若无装置E,则实验测定的$\frac{x}{y}$的值将偏小(选填“偏大”、“偏小”或“无影响”).
②某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量56.0g
C.装置C实验后增重9.0g
D.装置D实验后增重8.8g
为测定$\frac{x}{y}$的值,请你选用合适数据进行计算,并根据你的计算结果,写出该样品组成的化学式.
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2•CuCO3.某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50mol•L-1的Cu(NO3)2溶液、2.0mL 0.50mol•L-1的NaOH溶液和0.25mol•L-1的Na2CO3溶液按表Ⅰ所示体积混合.
实验2:将合适比例的混合物在表Ⅱ所示温度下反应.
实验记录如下:
| 编号 | V (Na2CO3)/mL | 沉淀情况 | 编号 | 反应温度/℃ | 沉淀情况 | |
| 1 | 2.8 | 多、蓝色 | 1 | 40 | 多、蓝色 | |
| 2 | 2.4 | 多、蓝色 | 2 | 60 | 少、浅绿色 | |
| 3 | 2.0 | 较多、绿色 | 3 | 75 | 较多、绿色 | |
| 4 | 1.6 | 较少、绿色 | 4 | 80 | 较多、绿色(少量褐色) |
①实验室制取少许孔雀石,应该采用的最佳条件是n[Cu(NO3)2]:n(Na2CO3)=2:1,75℃.
②80℃时,所制得的孔雀石有少量褐色物质的可能原因是Cu(OH)2受热分解为CuO.
(2)实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用如图所示的装置(夹持仪器省略)进行实验:

步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中.
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量.
步骤3:加热装置B直至装置C中无气泡产生.
步骤4:(请补充该步操作内容).
步骤5:称量相关装置的质量.
①装置A的作用是;若无装置E,则实验测定的$\frac{x}{y}$的值将偏小(选填“偏大”、“偏小”或“无影响”).
②某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量56.0g
C.装置C实验后增重9.0g
D.装置D实验后增重8.8g
为测定$\frac{x}{y}$的值,请你选用合适数据进行计算,并根据你的计算结果,写出该样品组成的化学式.
14.下列说法中不正确的是( )
①乙烯的结构简式可以表示为CH2CH2
②苯、乙醇和乙酸都能发生取代反应
③油脂都不能使溴的四氯化碳溶液褪色
④沼气和天然气的主要成分都是甲烷
⑤石油分馏可获得乙酸、苯及其衍生物
⑥糖类、蛋白质、聚乙烯都属于高分子化合物
⑦煤经气化和液化两个物理变化过程,可变为清洁能源.
①乙烯的结构简式可以表示为CH2CH2
②苯、乙醇和乙酸都能发生取代反应
③油脂都不能使溴的四氯化碳溶液褪色
④沼气和天然气的主要成分都是甲烷
⑤石油分馏可获得乙酸、苯及其衍生物
⑥糖类、蛋白质、聚乙烯都属于高分子化合物
⑦煤经气化和液化两个物理变化过程,可变为清洁能源.
| A. | 除①③⑤外 | B. | 除②④外 | C. | 除①⑥⑦外 | D. | 除②④⑦外 |
11.下列实验中,对应的现象以及结论都正确的是( )
| A. | 向碳酸钠与碳酸氢钠的混合溶液逐滴滴入盐酸溶液,立即产生大量气泡 | |
| B. | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明该溶液中有SO42- | |
| C. | 常温下,向0.1mol/L NaF和pH=12 NaOH的混合溶液中,滴加MgCl2溶液,先生成 MgF2沉淀(已知K[Mg(OH)]2=7.4×10-11 K( MgF2)=5.6×10-12) | |
| D. | 向 Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,则溶液变黄,说明氧化性H2O2>Fe3+ |
18.下列离子方程式中,正确的是( )
| A. | 向水中加入金属钠:Na+H2O═Na++OH-+H2↑ | |
| B. | 用NaOH溶液检验NH4Cl溶液中的铵根离子:NH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2Cl- | |
| D. | 用食醋除去水瓶中的水垢:CO${\;}_{3}^{2-}$+2CH3COOH═2CH3COO-+CO2↑+H2O |
15.下列两种物质作用时,反应条件或反应物的用量比改变,生成的化合物不会改变的( )
| A. | 钠与氧气 | B. | 氢氧化钠与二氧化碳反应 | ||
| C. | 氧化钠与水反应 | D. | 木炭(C)和O2 |
2.理论上不能用于设计成原电池的反应是( )
| A. | HCl+NaOH═NaCl+H2O△H<0 | |
| B. | 2CH3OH(l)+3O2(g)$\stackrel{点燃}{→}$2CO2(g)+4H2O(l)△H<0 | |
| C. | 4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)△H<0 | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H<0 |