��Ŀ����
17�����ʯ��һ�����ڽ���װ�εĹ����ο����֪ij�س����ķ��ʯ�ɿ�������Ҫ�ɷֹ���ͭ��X•3H2O��Ħ������=334g/mol���뺬����������Y��ͬ��ɣ�X��Y��������Ԫ�أ���ҵ���������������Ʊ�ͭ�Σ�����Һ���е���KSCN��Һ��Ѫ��ɫ��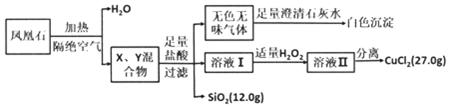
��ش�
��1������Y�г���������е�Ԫ��ΪFe��C����Ԫ�ط��ţ���x�Ļ�ѧʽΪCu2Si2O6��2CuO•2SiO2��
��2���������Һ���м�������H2O2�����������ݲ������й۵���Ϊ��Y�е�ijԪ�����ӽ�H2O2���������£�д����Ӧ�����ӷ���ʽ2Fe3++H2O2=2Fe2++2H++O2����
���� ���ʯ�ɿ�������Ҫ�ɷֹ���ͭ��X•3H2O��Ħ������=334g/mol���뺬����������Y��ͬ��ɣ�X��Y��������Ԫ�أ�����Һ���е���KSCN��Һ��Ѫ��ɫ˵����Һ���к�Fe3
+���ӣ���Һ���к�Fe2+���ӣ����ʯ�����������ȷֽ�����ˮ��X��Y�Ļ���������м�������������˵õ���ɫ��ζ����ͨ����������ʯ��ˮ���ɰ�ɫ����֤������ΪCO2��֤��YΪ̼���Σ��õ���Һ�����������������õ���Һ����KSCN��Һ��Ѫ��ɫ��˵����Һ���к�Fe3+���ӣ���Һ���к�Fe2+���ӣ�֤��Y�Ǻ�����̼��������Ԫ�ص��Σ���������CuCl2����27.0g�����ʵ���n��CuCl2��=$\frac{27.0g}{135g/mol}$=0.2mol��SiO2����12.0g�����ʵ���n��SiO2��=$\frac{12.0g}{60g/mol}$=0.2mol��n��Cu����n��Si��=0.2��0.2=1��1������ͭ��X•3H2OĦ������=334g/mol��XĦ������=344g/mol-3��18g/mol=280��/mol����n��Cu��=n��Si��=2=2��n��O��=6���õ�XΪCu2Si2O6���ݴ˷����жϣ�
��� �⣺���ʯ�ɿ�������Ҫ�ɷֹ���ͭ��X•3H2O��Ħ������=334g/mol���뺬����������Y��ͬ��ɣ�X��Y��������Ԫ�أ�����Һ���е���KSCN��Һ��Ѫ��ɫ˵����Һ���к�Fe3+���ӣ���Һ���к�Fe2+���ӣ����ʯ�����������ȷֽ�����ˮ��X��Y�Ļ���������м�������������˵õ���ɫ��ζ����ͨ����������ʯ��ˮ���ɰ�ɫ����֤������ΪCO2��֤��YΪ̼���Σ��õ���Һ�����������������õ���Һ����KSCN��Һ��Ѫ��ɫ��˵����Һ���к�Fe3+���ӣ���Һ���к�Fe2+���ӣ�֤��Y�Ǻ�����̼��������Ԫ�ص��Σ���������CuCl2����27.0g�����ʵ���n��CuCl2��=$\frac{27.0g}{135g/mol}$=0.2mol��SiO2����12.0g�����ʵ���n��SiO2��=$\frac{12.0g}{60g/mol}$=0.2mol��n��Cu����n��Si��=0.2��0.2=1��1������ͭ��X•3H2OĦ������=334g/mol��XĦ������=344g/mol-3��18g/mol=280��/mol����n��Cu��=n��Si��=2=2��n��O��=6���õ�XΪCu2Si2O6��
��1������Y�г���������е�Ԫ��ΪFe��C����������X��ѧʽΪ��Cu2Si2O6��2CuO•2SiO2��
�ʴ�Ϊ��Fe��C�� Cu2Si2O6��2CuO•2SiO2��
��2�������Һ���м�������H2O2�����������ݲ������й۵���Ϊ��Y�е�ijԪ�����ӽ�H2O2���������£�������ֻ֪��Fe3+���������ԣ���Ӧ�����ӷ���ʽΪ��2Fe3++H2O2=2Fe2++2H++O2����
�ʴ�Ϊ��2Fe3++H2O2=2Fe2++2H++O2����
���� ���⿼��������ת����������ɷ�������ѧʽ����ȷ�������ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д� ���������ν�ϵ�д�
���������ν�ϵ�д�| ���� | �¶�/�� | ���ʵ���ʼŨ��/mol•L-1 | ���ʵ�ƽ��Ũ��/mol•L-1 | ||
| c��SO2�� | c��O2�� | c��SO3�� | c��SO3�� | ||
| �� | 758 | 0.2 | 0.1 | 0 | 0.044 |
| �� | 758 | 0.1 | 0.05 | 0 | |
| �� | 858 | 0.2 | 0.1 | 0 | |
| A�� | �ӿ�ʼ��ƽ��ʱ����������SO3�ķ�Ӧ����Ϊ0.044 mol•L-1•s-1 | |
| B�� | ƽ��ʱ����������SO3��Ũ��С��0.022 mol•L-1 | |
| C�� | ƽ��ʱ����������SO3��Ũ�ȴ���0.044 mol•L-1 | |
| D�� | ����ʼʱ�����������г���0.02 mol SO2��0.01 mol O2��0.02 mol SO3����Ӧ���淴Ӧ������� |
| A�� | �٢ڢۢ� | B�� | ֻ�Тڢۢ� | C�� | ֻ�Т٢ڢ� | D�� | ֻ�Тڢ� |
| A�� | 0.5 mol O2����ԭ����Ϊ0.5NA | B�� | 1.8 g��NH4+�к��еĵ�����ΪNA | ||
| C�� | 48 g O3���е���ԭ����ΪNA | D�� | 1 mol H2O2�к�NA��H2��NA��O2 |
| A�� | 1 mol NH3�����еĵ�����Ϊ 17NA | |
| B�� | ���³�ѹ�£�22.4 L ����������ԭ����Ϊ 2NA | |
| C�� | ���³�ѹ�£�48g O3 ��������ԭ����Ϊ 3NA | |
| D�� | 1 mol/L NaCl ��Һ�������� Na+��Ϊ NA |
| A�� | N2��NO | B�� | HNO3��NO | C�� | BaCl2��BaSO4 | D�� | Fe2+��Fe3+ |

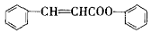 ���Ǻϳɸ߾۷�����ԭ�ϣ���ϳ�·�ߣ����ַ�Ӧ������ȥ����ͼ��ʾ��
���Ǻϳɸ߾۷�����ԭ�ϣ���ϳ�·�ߣ����ַ�Ӧ������ȥ����ͼ��ʾ��
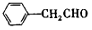 ��
��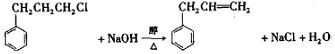 ��
�� ��
�� ��
��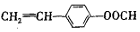 ������дһ�֣�
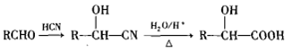
������дһ�֣�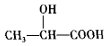 ���ĺϳ�·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������
���ĺϳ�·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������