题目内容
20.“化学是一门中心学科,与社会发展的需要有密切的关系”.下列有关叙述不正确的是( )| A. | 为了防止食品受潮及富脂食品氧化变质,常在包装袋中放入硅胶和硫酸亚铁( ) | |
| B. | 积极推行和使用能被微生物降解的新型聚合物材料 | |
| C. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| D. | 废旧电池应集中回收,不能填埋处理 |
分析 A.根据硅胶和硫酸亚铁的性质分析;
B.积极推行和使用能被微生物降解的新型聚合材料,可以减少白色污染;
C.依据绿色化学的核心解答;
D.根据废旧电池所含的少量的重金属对人体有害,应该集中回收处理判断.
解答 解:A.为了防止食品受潮及氧化变质,一般防受潮放硅胶,防氧化腐烂变质应放还原铁粉或亚铁盐,故A正确;
B.积极推行和使用能被微生物降解的新型聚合材料,可以减少白色污染,利于节能减排、改善环境质量,故B正确;
C.绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染,故C错误;
D.废旧电池所含的少量的重金属对人体有害,应该集中回收处理,不能填埋处理,故D正确;
故选:C.
点评 本题考查了化学与生活,设计食品的保存、环境污染与治理,明确物质的性质是解题关键,注意对相关知识的积累,题目难度不大.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
15.常温下20滴水为1mL,水的密度为1g/mL,每滴水含有a个水分子,则阿伏德罗常数可表示为( )
| A. | a | B. | 2a | C. | 18a | D. | 360a |
12. 以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ/mol
①该反应在高温下能自发进行的原因是△S>0
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是BDF(填字母,下同).
A.容器中的压强不变 B.1mol H-H 键断裂的同时断裂2mol H-O 键
C.V (CO)=V (H2)D.密闭容器的容积不再改变
E.消耗1mol 水的同时生成1mol H2 F.容器的密度不变
③该反应的平衡常数的表达式K=$\frac{c(CO)•c({H}_{2})}{c({H}_{2}O)}$.
(2)水煤气再进一步反应可制取氢气.反应为H2O(g)+CO(g)?H2(g)+CO2(g),某温
度下该反应的逆反应平衡常数K=$\frac{4}{9}$.该温度下在甲、乙、丙三个恒容密闭容器中,只
投入H2(g)和CO2(g),其起始浓度如下表所示.下列判断不正确的是B.
A.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
B.平衡时,甲中和丙中H2的转化率不等
C.平衡时,丙中c(CO2)是甲中的2 倍
D.平衡时,乙中CO2的转化率大于60%
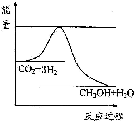
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.在体积为1L 的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c (CH3OH)减小的是A.
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来 D.再充入1mol CO2 和3mol H2.
 以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ/mol
①该反应在高温下能自发进行的原因是△S>0
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是BDF(填字母,下同).
A.容器中的压强不变 B.1mol H-H 键断裂的同时断裂2mol H-O 键
C.V (CO)=V (H2)D.密闭容器的容积不再改变
E.消耗1mol 水的同时生成1mol H2 F.容器的密度不变
③该反应的平衡常数的表达式K=$\frac{c(CO)•c({H}_{2})}{c({H}_{2}O)}$.
(2)水煤气再进一步反应可制取氢气.反应为H2O(g)+CO(g)?H2(g)+CO2(g),某温
度下该反应的逆反应平衡常数K=$\frac{4}{9}$.该温度下在甲、乙、丙三个恒容密闭容器中,只
投入H2(g)和CO2(g),其起始浓度如下表所示.下列判断不正确的是B.
| 起始 浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
B.平衡时,甲中和丙中H2的转化率不等
C.平衡时,丙中c(CO2)是甲中的2 倍
D.平衡时,乙中CO2的转化率大于60%
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.在体积为1L 的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c (CH3OH)减小的是A.
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来 D.再充入1mol CO2 和3mol H2.
9.下列图示实验正确的是( )
| A. | 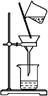 除去粗盐溶液中的不溶物 | B. |  碳酸氢钠受热分解 | ||
| C. | 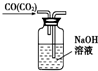 除去CO气体中的CO2气体 | D. | 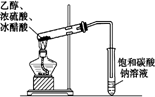 乙酸乙酯制备演示实验 |
10.
I:(1)第三周期元素M的电离能情况如甲图A所示.则M元素的价层电子排布式是3s2
(2)图B折线c(选填“a”、“b”或“c”)可以表达出第ⅣA族元素氢化物的沸点的变化规律.其中点A表示的分子的化学式为H2O,其沸点较高是因为水分子间可以形成氢键.
(3)COCl2 俗称光气,分子中C原子采取sp2杂化成键;其中分子中的共价键含有C(填序号):
A 2个σ键 1个π键 B 2个键π C 3个σ键、1个π键
Ⅱ:海水中富含氯元素.
(4)KCl广泛应用于医药和农业,KCl晶体中基态的Cl-电子排布式为1s22s22p63s23p6
(5)下列是IA族的Li、Na、K三种金属元素的电离能
则三种金属的氯化物(RCl)的熔点由高到低的顺序为LiCl>NaCl>KCl(用化学式回答),原因是随核电荷数增大,阳离子半径增大,晶格能减小,熔点降低
(6)RCl用作有机机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M 三个电子层,它与Cl-形成的晶体结构如图乙所示.R的元素符号是Cu,每个Cl-周围最近的Cl-12个.已知该晶体密度为1.15 g/cm3,则晶胞中最近的R+和Cl-之间的距离为$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{4×99.5}{1.15×6.02×1{0}^{23}}}$cm(NA=6.02×1023/mol,只写出计算表达式即可)

I:(1)第三周期元素M的电离能情况如甲图A所示.则M元素的价层电子排布式是3s2
(2)图B折线c(选填“a”、“b”或“c”)可以表达出第ⅣA族元素氢化物的沸点的变化规律.其中点A表示的分子的化学式为H2O,其沸点较高是因为水分子间可以形成氢键.
(3)COCl2 俗称光气,分子中C原子采取sp2杂化成键;其中分子中的共价键含有C(填序号):
A 2个σ键 1个π键 B 2个键π C 3个σ键、1个π键
Ⅱ:海水中富含氯元素.
(4)KCl广泛应用于医药和农业,KCl晶体中基态的Cl-电子排布式为1s22s22p63s23p6
(5)下列是IA族的Li、Na、K三种金属元素的电离能
| X | Y | Z | |
| 第一电离能(KJ/mol) | 526.2 | 502.8 | 425.2 |
(6)RCl用作有机机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M 三个电子层,它与Cl-形成的晶体结构如图乙所示.R的元素符号是Cu,每个Cl-周围最近的Cl-12个.已知该晶体密度为1.15 g/cm3,则晶胞中最近的R+和Cl-之间的距离为$\frac{\sqrt{3}}{4}$×$\root{3}{\frac{4×99.5}{1.15×6.02×1{0}^{23}}}$cm(NA=6.02×1023/mol,只写出计算表达式即可)
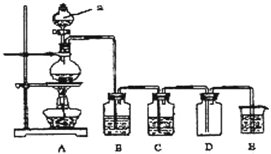 如图是实验室中制备气体或验证气体性质的装置图
如图是实验室中制备气体或验证气体性质的装置图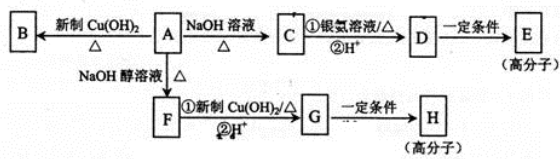
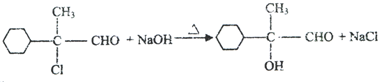 .
.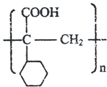 ,E的结构简式是
,E的结构简式是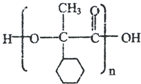 .
. 钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为:2Mn2++5S2O82-+8H2O$\frac{\underline{\;Ag+\;}}{\;}$2MnO4-+10SO42-+16H+
钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为:2Mn2++5S2O82-+8H2O$\frac{\underline{\;Ag+\;}}{\;}$2MnO4-+10SO42-+16H+