题目内容
【题目】甲苯(![]() )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(![]() )、苯甲酸(
)、苯甲酸(![]() )等产品。下表列出了有关物质的部分物理性质,请回答:
)等产品。下表列出了有关物质的部分物理性质,请回答:
名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度(ρ水=1g·cm-3) | 溶解性 | |
水 | 乙醇 | |||||
甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
注:甲苯、苯甲醛、苯甲酸三者互溶。
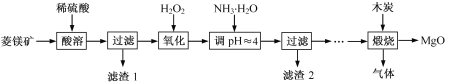
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸(作为溶剂)和2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。

(1)装置a的名称是___。
(2)三颈瓶中发生反应的化学方程式为___。
(3)写出苯甲醛与银氨溶液在一定的条件下发生反应的化学方程式:___。
(4)反应完毕后,反应混合液经过自然冷却至室温时,还应经过___、___(填操作名称)等操作,才能得到苯甲醛粗产品。
(5)实验中加入过量过氧化氢且反应时间较长,会使苯甲醛产品中产生较多的苯甲酸。若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是___(按步骤顺序填字母)。
a.对混合液进行分液
b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2
d.加入适量碳酸氢钠溶液混合振荡
【答案】(球形)冷凝管 ![]() +2H2O2
+2H2O2![]()
![]() +3H2O
+3H2O  +2Ag(NH3)2OH
+2Ag(NH3)2OH +2Ag↓+H2O+3NH3 过滤 蒸馏 dacb
+2Ag↓+H2O+3NH3 过滤 蒸馏 dacb
【解析】
(1)~(3)以冰醋酸为溶剂,在固体催化剂的作用下,甲苯在70℃时被过氧化氢氧化,生成苯甲醛等,苯甲醛含有醛基,能被银氨溶液氧化生成苯甲酸铵、银等。
(4)~(5)反应生成的苯甲醛溶解在冰醋酸、甲苯的混合液中,催化剂为不溶性固体,所以需先分离出液态有机物,然后再分离液态混合物得到粗苯甲醛。苯甲酸和苯甲醛都为固体,为获得苯甲酸,可先加入碱性溶液将苯甲酸转化为可溶物,然后分液;再往水层中加酸,让苯甲酸结晶析出,最后过滤分离。
(1)装置a用于将蒸气冷凝,其名称是(球形)冷凝管。答案为:(球形)冷凝管;
(2)三颈瓶中甲苯在催化剂作用下被H2O2氧化为苯甲醛和水,发生反应的化学方程式为![]() +2H2O2
+2H2O2![]()
![]() +3H2O。答案为:
+3H2O。答案为:![]() +2H2O2
+2H2O2![]()
![]() +3H2O;
+3H2O;
(3)苯甲醛与银氨溶液在一定条件下发生反应,生成苯甲酸铵、银沉淀等,化学方程式为: +2Ag(NH3)2OH
+2Ag(NH3)2OH +2Ag↓+H2O+3NH3。答案为:
+2Ag↓+H2O+3NH3。答案为: +2Ag(NH3)2OH
+2Ag(NH3)2OH +2Ag↓+H2O+3NH3;
+2Ag↓+H2O+3NH3;
(4)反应完毕后,反应混合液经过自然冷却至室温时,需先将固、液分离,再从液体混合物中提取苯甲醛,所以还应经过过滤、蒸馏等操作,才能得到苯甲醛粗产品。答案为:过滤;蒸馏;
(5)从混有苯甲酸的苯甲醛中分离出苯甲酸,应先将混合液溶于适量碳酸氢钠溶液,然后将混合液分液;往水层中加入盐酸调节pH=2,此时苯甲酸结晶析出,再过滤、洗涤、干燥,便可获得苯甲酸,正确的操作步骤是dacb。答案为:dacb。

【题目】丙烷、乙烯等有机物在工业上有广泛的应用,回答下列问题:
(1)已知:①C3H8(g)+5O2(g)= 3CO2(g)+4H2O(l) △H1
②C(石墨,s)+O2(g)= CO2(g) △H2
③2H2(g)+O2(g)= 2H2O(l) △H3
写出丙烷气体(C3H8)分解得到石墨(C)和氢气的热化学方程式:___。
(2)煤制乙烯包括合成气制备、合成气制甲醇、甲醇分解三步,则:
①生产合成气的反应:C(s)+H2O(g)=CO(g)+H2(g)在高温下能自发进行,则该反应的___(填选项)。
a.△H>0 △S>0 b.△H>0 △S<0
c.△H<0 △S>0 d.△H>0 △S<0
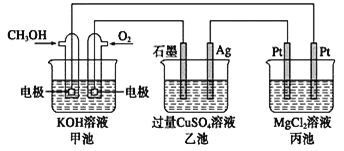
②用合成气制备甲醇的反应为:CO(g)+ 2H2(g)![]() CH3OH(g)(不发生其他反应)。四个容器中起始时压强、容积均相同,维持恒温,控制条件如下表;
CH3OH(g)(不发生其他反应)。四个容器中起始时压强、容积均相同,维持恒温,控制条件如下表;
编号 | 条件控制 | CO(g)/moL | H2(g)/moL | CH3OH(g)/moL |
A | 维持恒容 | 0.2 | 0.4 | 0 |
B | 维持恒容 | 0.1 | 0.2 | 0.1 |
C | 维持恒容 | 0.4 | 0.8 | 0 |
D | 维持恒压 | 0.4 | 0.8 | 0 |
达到平衡时,四个容器中甲醇的体积分数由大到小的关系是___(用字母表示)。
(3)在两个容积均为1L的密闭容器中以不同的氢碳比[n(H2)/n(CO2)]充入H/span>2和CO2,在一定条件下发生反应:2CO2(g)+ 6H2(g)![]() C2H4(g)+ 4H2O(g)△H。CO2的平衡转化率α(CO2)与温度的关系如图所示。
C2H4(g)+ 4H2O(g)△H。CO2的平衡转化率α(CO2)与温度的关系如图所示。
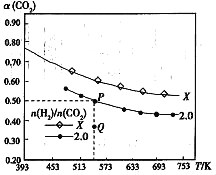
①此反应的平衡常数表达式K=___,P点对应温度下,K的值为___。
②该反应的△H___0(填“>”“<”或“=”),判断的理由是___。
③氢碳比:X___2.0(填“>”“<”或“=”)。
④在氢碳比为2.0时,Q点v(逆)___P点的v(逆)(填“>”“<”或“=”)。