题目内容
9.关于由锌、铜和稀硫酸构成的原电池的下列说法中正确的是( )| A. | 锌是负极,铜是正极 | B. | 电子从铜片经导线流向锌片 | ||
| C. | 负极的反应式为2H++2e-=H2 | D. | 反应一段时间后,溶液的酸性增强 |
分析 锌比铜活泼,形成原电池反应时,锌为负极,发生氧化反应,铜为正极,正极上氢离子得电子发生还原反应,电子从负极流向正极,以此解答.
解答 解:A.锌比铜活泼,应为原电池的负极,发生氧化反应,铜为正极,发生还原反应,则A正确;
B.电子从负极流向正极,则电子从锌片经导线流向铜片,故B错误;
C.锌为负极,发生氧化反应,负极的反应式为Zn-2e-═Zn2+,故C错误;
D.正极上氢离子得电子发生还原反应,则氢离子浓度减小,所以反应一段时间后,溶液的酸性减弱,故D错误.
故选A.
点评 本题考查原电池池知识,侧重于学生的分析能力和电化学知识的综合考查,注意把握电极方程式的书写,难度不大.

练习册系列答案
相关题目
10.化学与科学、技术、社会、环境密切相关.下列说法不正确的是( )
| A. | SiO2是酸性氧化物,但不能直接与水反应生成H2SiO3 | |
| B. | 常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸 | |
| C. | 氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 | |
| D. | Na2O2能与CO2反应产生O2,可用作呼吸面具的供氧剂 |
11.根据如图判断,下列说法正确的是( )
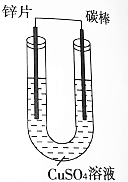

| A. | 该过程化学能转化为热能 | |
| B. | 该反应过程中只有化学键形成,没有化学键断裂 | |
| C. | CuSO4溶液里Cu2+移向负极 | |
| D. | 可以用铜片代替碳棒 |
17.下列各组中的反应,属于同一反应类型的是( )
| A. | 由溴乙烷制乙醇;由乙烯与水反应制乙醇 | |
| B. | 乙烯使溴的CCl4溶液褪色;甲苯使酸性高锰酸钾溶液褪色 | |
| C. | 由苯制硝基苯;由环己醇制环己烯 | |
| D. | 由乙酸和乙醇制乙酸乙酯;苯与液溴在FeBr3催化下制溴苯 |
4.下列物质互为同系物的一组是( )
| A. | 乙醇和乙酸 | B. | 甲烷和丙烷 | C. | 金刚石与石墨 | D. | 16O和18O |
14.某物质加入到溴水中振荡混合,静置后分为两层,上层几乎呈无色,该物质是( )
| A. | 酒精溶液 | B. | 四氯化碳 | C. | 碘化钾溶液 | D. | 食盐水 |
1.下列物质中可用于雕刻玻璃的是( )
| A. | 盐酸 | B. | 氢氟酸 | C. | 烧碱 |
19.下列说法正确的是( )
| A. | 煤是无机化合物,天然气和石油是有机化合物 | |
| B. | 利用化石燃料燃烧放出的热量使分解产生氢气,是氢能开发的研究方向 | |
| C. | 化学电源放电、植物光合作用都能发生化学变化,但没有能量的转化 | |
| D. | 若化学过程中断开化学键吸收的能量大于形成化学键所放出的能量,则反应吸热 |