题目内容
 在试管A中加入3mL 乙醇,然后边振荡试管边慢慢加入2mL 浓硫酸和2mL 乙酸,按如图所示连接好装置进行实验,以制取乙酸乙酯.
在试管A中加入3mL 乙醇,然后边振荡试管边慢慢加入2mL 浓硫酸和2mL 乙酸,按如图所示连接好装置进行实验,以制取乙酸乙酯.(1)试管B中盛放的溶液是
(2)乙醇乙酸反应的化学方程式是:
(3)实验完成后,试管B的液面上有透明的不溶于水的油状液体产生.若分离B中的液体混合物需要用到的玻璃仪器主要是
考点:乙酸乙酯的制取
专题:
分析:(1)乙醇与乙酸都易挥发,制备的乙酸乙酯含有乙醇与乙酸,通常用饱和碳酸钠溶液吸收乙酸乙酯,中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯;
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为取代反应;
(3)分离互不相溶的液体,应采取分液操作,常用的仪器是分液漏斗.
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为取代反应;
(3)分离互不相溶的液体,应采取分液操作,常用的仪器是分液漏斗.
解答:
解:(1)乙醇与乙酸都易挥发,制备的乙酸乙酯含有乙醇与乙酸,通常用饱和碳酸钠溶液吸收乙酸乙酯,中和挥发出来的乙酸,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯,故答案为:饱和碳酸钠溶液;中和挥发出来的乙酸,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯;
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的化学方程式为
CH3COOH+CH3CH2OH
CH3COOC2H5+H2O,故答案为:CH3COOH+CH3CH2OH
CH3COOC2H5+H2O;
(3)分离互不相溶的液体,应采取分液操作,常用的仪器是分液漏斗;故答案为:分液漏斗.
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的化学方程式为
CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
(3)分离互不相溶的液体,应采取分液操作,常用的仪器是分液漏斗;故答案为:分液漏斗.
点评:本题主要考查乙酸乙酯的制备,难度不大,注意实验混合液的配制、饱和碳酸钠溶液的作用以及酯化反应的机理.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
在2L的密闭容器中,发生如下反应:3A(g)+B(g)?2C(g)+D(g),若最初加入的A和B都是4mol,在前10s内A的平均反应速率为0.12mol?L-1?s-1,则10s时,容器内B的物质的量为( )
| A、3.6 mol |
| B、3.2 mol |
| C、2.4 mol |
| D、1.2 mol |
属于碱性氧化物的是( )
| A、SO2 |
| B、H2O |
| C、Na2O |
| D、CaSiO3 |
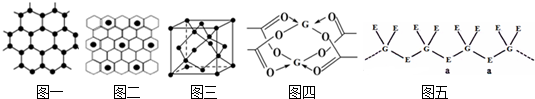
 ”表示),原子分布如图二所示,该物质的化学式为
”表示),原子分布如图二所示,该物质的化学式为 )该反应的原子利用率为100%,反应的化学方程式为
)该反应的原子利用率为100%,反应的化学方程式为 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如图
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如图