题目内容
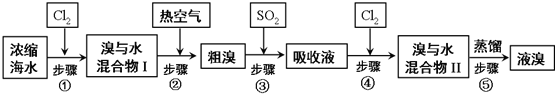
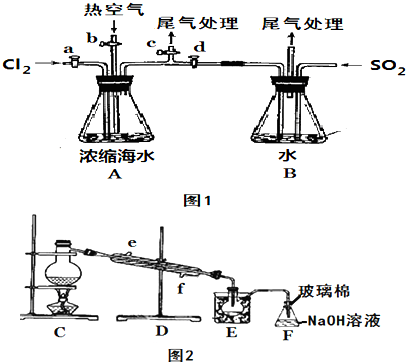
16.写出下列序号对应的反应
①
 ②
② ③
③ ④
④ .
.
分析 有机物含有碳碳双键,进而与溴发生加成反应,含有羟基,可发生钠反应生成氢气,与乙酸发生酯化反应,在浓硫酸作用下,可与硝酸发生取代反应生成硝基化合物,以此解答该题.
解答 解:①有机物含有碳碳双键,进而与溴发生加成反应,反应的方程式为 ,
,
故答案为: ;
;
②有机物含有羟基,与乙酸发生酯化反应,方程式为 ,
,
故答案为: ;
;
③在浓硫酸作用下,可与硝酸发生取代反应生成硝基化合物,方程式为 ,
,
故答案为: ;
;
④含有羟基,可发生钠反应生成氢气,方程式为 ,
,
故答案为: .
.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,为解答该题的关键,难度中等.

练习册系列答案
相关题目
6.在标准状况下将11.2L乙烯和乙炔的混合气体通入足量溴水中充分反应,测得有128g溴参加了反应,则乙烯和乙炔的物质的量之比为( )
| A. | 2:3 | B. | 1:2 | C. | 3:4 | D. | 4:5 |
7.化合物A、B是中学常见的物质,其阴、阳离子只能从表中选择:
(1)若A、B的水溶液均为无色,且A的水溶液呈强酸性,B的水溶液呈强碱性.混合后产生不溶于稀盐酸的白色沉淀及能使湿润的红色石蕊试纸变蓝色的气体.
①B的化学式为Ba(OH)2.
②A、B溶液混合加热反应的离子方程式H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化.则
①A的化学式为FeI2.
②经分析上述过程中溶液变黄的原因可能有两种(用离子方程式表示)
Ⅰ8H++2NO3-+6I-=2NO↑+3I2+4H2O;Ⅱ8H++2NO3-+6I-=2NO↑+3I2+4H2O和4H++NO3-+3Fe2+=NO↑+3Fe3++2H2O.
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理(其他合理亦可).
| 阳离子 | K+、Na+、Fe2+、Ba2+、NH4+、Ca2+ |
| 阴离子 | OH-、NO3-、I-、HCO3-、AlO2-、HSO4- |
①B的化学式为Ba(OH)2.
②A、B溶液混合加热反应的离子方程式H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化.则
①A的化学式为FeI2.
②经分析上述过程中溶液变黄的原因可能有两种(用离子方程式表示)
Ⅰ8H++2NO3-+6I-=2NO↑+3I2+4H2O;Ⅱ8H++2NO3-+6I-=2NO↑+3I2+4H2O和4H++NO3-+3Fe2+=NO↑+3Fe3++2H2O.
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理(其他合理亦可).
4.北京奥运会“祥云”火炬使用的燃料为丙烷.下列关于丙烷的说法正确的是( )
| A. | 分子中的碳原子在一条直线上 | B. | 其一氯代物只有一种 | ||
| C. | 能使酸性高锰酸钾溶液褪色 | D. | 结构简式为CH3 CH2 CH3 |
1.下列离子方程式书写正确的是( )
| A. | 实验室利用熟石灰和氯化铵共热制取氨气:NH4++OH--$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| B. | 用食醋浸泡热水瓶中的水垢(CaCO3):CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| D. | 向Na2SO3溶液中滴加足量NaClO溶液:SO32-+ClO-═SO42-+Cl- |
5.设NA为阿伏伽德罗常数,下列关于1L 0.2mol•L-1的Mg(NO3)2溶液的说法不正确的是( )
| A. | 2L溶液中阴、阳离子总数为1.2NA | |
| B. | 100mL溶液中NO3-物质的量为为0.4mol | |
| C. | 200mL溶液中Mg2+浓度为0.2mol•L-1 | |
| D. | 500mL溶液中NO3-总数为0.2NA |
15.下列各组物质中所含化学键类型完全相同的是( )
| A. | HBr和CO2 | B. | NH3和NH4Cl | C. | KOH和NaCl | D. | H2SO4和Na2SO4 |