题目内容
A元素的最高价离子0.5mol被还原成中性原子时得到6.02×1023个电子。当它与盐酸充分反应时放出0.02g氢气,消耗A单质0. 4g。B元素的原子核外电子层数与A相同,且B元素的单质常温下为深棕红色液体。
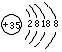
(1)画出A、B元素常见离子的结构示意图________________,________________。
(2)用电子式表示A、B形成化合物的过程__________,化学键为__________。
答案:
解析:
提示:
解析:
(1) Ca2+ (2)
|
提示:
据题意,0.5 mol A的最高价离子被还原成中性原子转移1 mol电子,说明A的最高化合价为+2价,肯定为金属元素。设A的相对原子质量为x。 A+2HCl == ACl2+H2↑ x 2 g 0.4 g 0.02 g
|

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目