题目内容
下列各组物质中,所有化学键都是共价键的是( )
| A、H2S和Na2O2 |
| B、H2O2和CaF2 |
| C、NH3和N2 |
| D、HNO3和NaCl |
考点:共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:一般来说,活泼金属元素与活泼非金属元素形成离子键,非金属之间形成共价键,以此来解答.
解答:
解:A.H2S含有共价键,Na2O2含有离子键和共价键,故A错误;
B.H2O2含有共价键,CaF2含有离子键,故B错误;
C.NH3和N2只含有共价键,故C正确;
D.HNO3含有共价键,NaCl含有离子键,故D错误.
故选C.
B.H2O2含有共价键,CaF2含有离子键,故B错误;
C.NH3和N2只含有共价键,故C正确;
D.HNO3含有共价键,NaCl含有离子键,故D错误.
故选C.
点评:本题考查化学键,注意把握化学键判断的一般规律即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列各组物质发生状态变化时都没有化学键的破坏的是( )
| A、食盐和蔗糖溶于水 |
| B、Cl2与HCl气体溶于水 |
| C、碘和干冰升华 |
| D、二氧化硅和氧化钠熔化 |
稀H2SO4、NaOH和Al为原料制取Al(OH)3,有下列三种不同的途径
甲:Al
Al2(SO4)3
Al(OH)3
乙:Al
NaAlO2
Al(OH)3
丙:
→Al(OH)3
已知:Al3++3AlO2-+6H2O═4Al(OH)3↓,若制取等量的Al(OH)3则( )
甲:Al
| H2SO4 |
| NaOH |
乙:Al
| NaOH |
| H2SO4 |
丙:
|
已知:Al3++3AlO2-+6H2O═4Al(OH)3↓,若制取等量的Al(OH)3则( )
| A、甲、乙消耗的原料同样多 |
| B、乙消耗的原料最少 |
| C、三者消耗的原料同样多 |
| D、丙消耗的原料最少 |
下列各离子或分子组能在水溶液中大量共存的是( )
| A、NH4+、H+、NO3-、Fe2+ |
| B、Fe3+、ClO-、Na+、AlO2- |
| C、CO32-、SO32-、Na+、Ba2+ |
| D、SO42-、Cl-、Na+、Al3+ |
对下列实验的描述正确的是( )
A、 图中所示的实验:根据检流计(G)中指针偏转的方向比较Zn、Cu的金属活泼性(检流计的偏转方向为电子流的流动方向) |
B、 图中所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀 |
C、 图中所示的实验:根据温度计读数的变化用浓硫酸和NaOH反应测定中和热 |
D、 图中所示的实验:根据两试管中溶液颜色的变化(热水中变蓝、冰水中变粉)判断Co(H2O)62+(蓝色)+4Cl-?CoCl42-(粉红色)+6H2O是放热反应 |
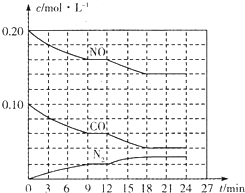 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
 中的手性碳原子
中的手性碳原子