题目内容
【题目】下列实验能实现的是( )
A. 图1装置左侧用于检验氯化铵受热分解出的氨气
图1装置左侧用于检验氯化铵受热分解出的氨气
B.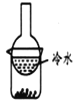 图2装置用于分离碘单质和高锰酸钾固体混合物
图2装置用于分离碘单质和高锰酸钾固体混合物
C.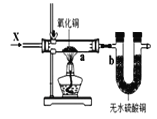 图3装置中若a处有红色物质生成,b处变蓝,证明X一定是H2
图3装置中若a处有红色物质生成,b处变蓝,证明X一定是H2
D. 图4装置可以制取少量CO2,安全漏斗可以防止气体逸出
图4装置可以制取少量CO2,安全漏斗可以防止气体逸出
【答案】D
【解析】
A、左侧的五氧化二磷会吸收氯化铵分解产生的氨气,因此左侧可检测氯化氢,故A不符合题意;
B、加热时碘升华,高锰酸钾会发生分解,因此加热法不能分离,故B不符合题意;
C、a处有红色物质生成,说明氧化铜被还原,b处变蓝,说明气体中含有水蒸气,因此有可能X中含有水蒸气,X也可能含有乙醇、氨气、甲烷等,故C不符合题意;
D、大理石和稀盐酸反应生成二氧化碳,安全漏斗可在左右侧形成液柱,可防止气体逸出,故D符合题意;
故答案为:D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
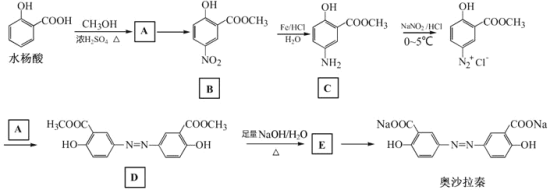
【题目】Bodensteins研究了下列反应:2HI(g)![]() H2(g)+I2(g)
H2(g)+I2(g)![]() 。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示。当升高温度,再次达到平衡时,v正 v逆可能落在A、B、C、D、E哪些点。
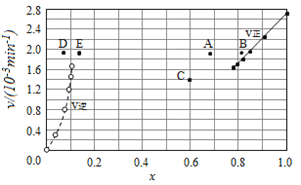
A. A D B. B D C. B E D. A E