��Ŀ����
����Ŀ�������Ϊ0.5L��AlCl3��Һ������ijŨ�ȵ�NaOH��Һ���õ��ij�����NaOH��Һ����ı仯����ͼ��ʾ�����н������ȷ����(����)
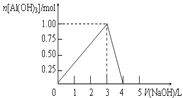
A. ��Ӧ�����У��������ʱ������Ϊ78g
B. ��Ӧ�����У�Al3+������1/3ת��ΪAl(OH) 3������������NaOH��Һ���������Ϊ3.5L
C. AlCl3��Һ��Ũ��Ϊ2.0mol/L
D. ��V(NaOH)��4.0Lʱ���õ�����Һ��Na����Cl��Ũ��һ�������
���𰸡�B
��������A����ͼ��֪���������Ϊ1.00mol��������Ϊ1mol��78g/mol=78g����A��ȷ��B����ͼ��֪���������Ϊ1.00mol��������Ԫ���غ㣬���Ժ���AlCl3�����ʵ�����1mol����Ӧ�����У�Al3+������![]() ת��ΪAl(OH)3��������
ת��ΪAl(OH)3��������![]() molAl3+ת��Ϊ����������ͼʾ�����ĵ����������������Ϊ1L��(3+
molAl3+ת��Ϊ����������ͼʾ�����ĵ����������������Ϊ1L��(3+![]() )L��������Ϊ3.5L����B����C����ͼ��֪����3LʱNaOHǡ����ȫ��Ӧ���ɳ�������Al3++3OH-=Al(OH)3������AlCl3��Һ��Ũ��Ϊ
)L��������Ϊ3.5L����B����C����ͼ��֪����3LʱNaOHǡ����ȫ��Ӧ���ɳ�������Al3++3OH-=Al(OH)3������AlCl3��Һ��Ũ��Ϊ![]() =2.0mol/L����C��ȷ��D����V(NaOH)=4.0Lʱ��������ȫ�ܽ⣬����ƫ�����ƺ�NaCl���õ�����Һ�к���Na+��AlO2-��Cl-�����ݵ���غ㣬Na+��Cl-Ũ��һ������ȣ���D��ȷ����ѡB��
=2.0mol/L����C��ȷ��D����V(NaOH)=4.0Lʱ��������ȫ�ܽ⣬����ƫ�����ƺ�NaCl���õ�����Һ�к���Na+��AlO2-��Cl-�����ݵ���غ㣬Na+��Cl-Ũ��һ������ȣ���D��ȷ����ѡB��

����Ŀ��Ŀǰ���ܽ��ȶ����ڵ��ȵ���������Cl2O��ClO2��Cl2O7�ȡ��й����ݼ��±���
��ѧʽ | Cl2O | ClO2 | Cl2O7 |
�е�/�� | 3.8 | 11.0 | 82.0 |
��ش��������⣺
(1)���¡���ѹ�£������������������������______________��
(2)Cl2O7�����������������ˮ��Ӧ�����ӷ���ʽ____________________________��
(3)ClO2��һ�ֳ��õ����������ҹ���2000��������ClO2��������������ˮ�����������ڶ�ˮ����ʱ��ClO2���ɽ�ˮ�е�Fe2����Mn2����ת����Fe(OH)3��MnO2���������ȥ��˵��ClO2����_____________�ԡ�
(4)��ҵ�Ͽ��������з�Ӧ�Ʊ�ClO2��2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4�����õ����ŷ�
��ʾ���÷�Ӧ����ת�Ƶķ������Ŀ______________��
(5)��ҵ���Ʊ�ClO2�ķ�Ӧԭ��Ϊ��
NaClO3+ HCl��Ũ��- ClO2��+ Cl2��+ H2O+ NaCl��
����ƽ����ʽ��______________��
��Ũ�����ڷ�Ӧ����ʾ������������__________________������ţ���
A����ԭ�� B�������� C������
����������Ӧ�в���0.1molClO2����ת�Ƶĵ�����Ϊ___________��
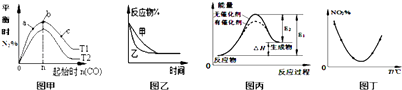
����Ŀ��һ���¶��£����������ԼΪ1.0L�ĺ����ܱ������з�����Ӧ��2CH3OH��g���TCH3OCH3��g��+H2O��g��������˵����ȷ���ǣ� ��
���� | �¶ȣ��棩 | ��ʼ���ʵ�����mol�� | ƽ�����ʵ�����mol�� | |
CH3OH��g�� | CH3OCH3��g�� | H2O��g�� | ||
I | 387 | 0.20 | 0.080 | 0.080 |
�� | 387 | 0.40 | ||
�� | 207 | 0.20 | 0.090 | 0.090 |
A.�÷�Ӧ������ӦΪ���ȷ�Ӧ
B.�ﵽƽ��ʱ������I�е�CH3OH����������������е�С
C.����I�з�Ӧ�ﵽƽ������ʱ����������еij�
D.����ʼʱ������I�г���CH3OH 0.1mol��CH3OCH30.15mol��H2O 0.10mol����Ӧ��������Ӧ�������