题目内容
化学研究性学习小组在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定.已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应).
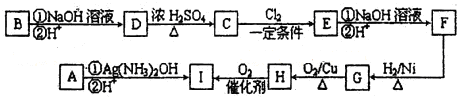
步骤一:电解精制:电解时,粗铜应与电源的 极相连.阴极上的电极反应式为 .
步骤二:电解完成后,该小组同学按如图流程对电解液进行处理:稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该反应的离子方程式: .

步骤一:电解精制:电解时,粗铜应与电源的
步骤二:电解完成后,该小组同学按如图流程对电解液进行处理:稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该反应的离子方程式:
考点:电解原理
专题:电化学专题
分析:电解精炼铜时,精铜做阴极,粗铜作阳极,阴极上是铜离子得电子;金属银可以和硝酸反应得到硝酸银以及水和一氧化氮,据此回答.
解答:
解:在电解精炼铜时,阳极反应是金属锌、铁、镍等先失电子,阴极上是铜离子得电子产生铜,Cu2++2e=Cu,精铜做阴极,粗铜作阳极,金属银可以和稀硝酸反应生成硝酸银、一氧化氮和水,即3Ag+4H++NO3-=3Ag++NO↑+2H2O,故答案为:正;Cu2++2e=Cu;3Ag+4H++NO3-=3Ag++NO↑+2H2O.
点评:本题涉及有关电解精炼铜、金属银的化学性质等综合知识,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中,正确的是( )
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中,正确的是( )| A、由TiO2制得1mol金属Ti,理论上外电路转移2 mol电子 |
| B、阳极的电极反应式为:C+2O2--4e-═CO2↑ |
| C、在制备金属钛前后,整套装置中CaO的总量减少 |
| D、若用铅蓄电池作该装置的供电电源,“+”接线柱应连接Pb电极 |
下列鉴别方法可行的是( )
| A、用氨水鉴别Al3+、Mg2+和Ag+ |
| B、用Ba(NO3)2溶液鉴别Cl-、SO42-和CO32- |
| C、用水鉴别乙醇、甲苯、硝基苯 |
| D、用KMnO4酸性溶液鉴别苯、甲苯、环己烷 |
某K2SO4样品中含有Na2SO4、KNO3和Ba(NO3)2三种杂质中的一种或两种.现称取17.4g样品于烧杯中加入足量水溶解,充分搅拌后得到澄清溶液.再往此澄清溶液加入过量的BaCl2溶液得到20g沉淀.对样品所含的杂质判断正确的是( )
| A、杂质一定不含KNO3 |
| B、杂质一定含有Ba(NO3)2可能还含有KNO3 |
| C、杂质一定不含Na2SO4 |
| D、杂质一定含KNO3可能还含有Na2SO4 |
下列叙述正确的是( )
| A、电解饱和食盐水制烧碱采用离子交换膜法,可以阻止阳离子通过 |
| B、在铁上镀锌时,锌棒作阴极,且电解液硫酸锌的浓度是不变的 |
| C、用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 |
| D、用惰性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1mol NaOH |
化学中的平衡:如化学平衡、溶解平衡、电离平衡.下列不存在平衡的是(不考虑水的电离平衡)( )
| A、稀醋酸溶液中 |
| B、氢氧化钙悬浊液中 |
| C、二氧化硫与氧气反应的混合物中 |
| D、稀氯化钠水溶液中 |
 氮是地球上极为丰富的元素.
氮是地球上极为丰富的元素.