题目内容
18.某工业上可采用以下步骤生产乙醇:
下列说法中不正确的是( )
| A. | 该过程中硫酸是催化剂 | B. | 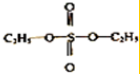 可属于二元酯 可属于二元酯 | ||
| C. | 该过程中①、②是加成反应 | D. | 该过程中③、④是水解反应 |
分析 A、从整个反应来看硫酸充当反应物;
B、依据酯类的定义分析判断即可;
C、乙烯中含碳碳碳双键,双键断开变成单键的反应为加成反应;
D、根据酯类水解的定义分析.
解答 解:A、催化剂的特点:“一变二不变”指:一变指:改变其他物质的化学反应速率;二不变指:催化剂的质量和化学性质不变,整个反应来看硫酸是反应物,不是催化剂,故A错误;
B、酸与醇生成酯,硫酸为二元酸,故此物质可以看作是二元酯,故B正确;
C、有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应,过程中①乙烯和硫酸发生加成反应、②③与硫酸发生加成反应,两者都是乙烯的加成反应,故C正确;
D.含氧酸与醇类发生酯化反应生成的有机产物为酯,C2H5OSO3H是硫酸乙酯、C2H5OSO3C2H5是硫酸二乙酯,两者都是酯类,该过程中③、④都是酯类的水解反应,故D正确;故选A.
点评 本题主要考查了乙烯的性质,题目难度不大,根据题目信息结合所学知识解答,注意催化剂的特点和判断方法.

练习册系列答案
相关题目
8. 反应N2O4(g)?2NO2(g);△H=+57kJ•mol-l,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法不正确的是( )
反应N2O4(g)?2NO2(g);△H=+57kJ•mol-l,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法不正确的是( )
 反应N2O4(g)?2NO2(g);△H=+57kJ•mol-l,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法不正确的是( )
反应N2O4(g)?2NO2(g);△H=+57kJ•mol-l,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法不正确的是( )| A. | A、C两点气体的平均相对分子质量:A>C | |
| B. | A、C两点气体的颜色:A深,C浅 | |
| C. | 由状态B到状态A,可以用加热的方法 | |
| D. | A、C两点的反应速率:A<C |
9.下列说法正确的是( )
| A. | 离子化合物中只能含离子键,不能有共价键 | |
| B. | 所有非金属之间形成的化学键一定是共价键 | |
| C. | 电子数相同的两种微粒一定是同一元素 | |
| D. | 共价化合物中一定无离子键 |
6.下列有关化学用语正确的是( )
| A. | -OH的电子式: | B. | 丁烷是键线式: | ||
| C. | 乙烯的结构简式:CH2=CH2 | D. | 最能反映甲烷真实结构的模型是: |
13.在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g)?2C(g)下列说法中能说明这一反应已经达到化学平衡状态的是( )
| A. | 生成C的速率与C分解的速率相等 | |
| B. | A、B、C的浓度相等 | |
| C. | 单位时间生成n molA,同时生成3n molB | |
| D. | A、B、C的分子数之比为1:3:2 |
3.某FeSO4、Fe2(SO4)3、H2SO4的混合溶液150mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6mol•L-1,则此溶液最多可溶解铁粉的质量( )
| A. | 11.2g | B. | 16.8g | C. | 19.6g | D. | 22.4g |
10.某有机物的结构简式如图,下列说法正确的是( )


| A. | 该有机物不能使酸性高锰酸钾溶液褪色 | |
| B. | 该有机物可发生加成、酯化和氧化反应 | |
| C. | 1mol该有机物最多可与2mol NaOH发生反应 | |
| D. | 该有机物的分子式为C11H18O3 |
7.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2LCCl4中含有的分子数为0.5NA | |
| B. | 1molCl2完全溶于水,转移的电子数为NA | |
| C. | 25℃时,PH=13的1.0LBa(OH)2溶液中含有的OH-数为0.1NA | |
| D. | 电解精炼铜,转移2NA个电子时,阳极溶解64g铜 |
8.用坩埚钳夹住一小块刚用酸处理过的铝箔,在酒精灯上加热至熔化,发现熔化的铝并不滴落.下列关于上述实验现象的解释不正确的是( )
| A. | 铝在空气中能很快形成氧化膜 | B. | 用酸处理时未能将氧化膜溶解 | ||
| C. | 氧化铝的熔点比铝高 | D. | 氧化铝薄膜包住了熔化的铝 |