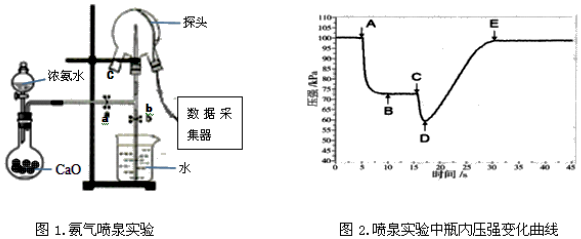
题目内容
3.体育比赛使用的发令枪中所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾.撞击时发生的化学反应方程式为:5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是( )| A. | 上述反应中氧化剂和还原剂的物质的量之比为5:6 | |
| B. | 产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成酸滴(雾) | |
| C. | 上述反应中消耗3molP时,转移电子的物质的量为15mol | |
| D. | 产物P2O5为酸性氧化物,但不是磷酸的酸酐 |
分析 A、反应5KClO3+6P═3P2O5+5KCl中,氧化剂是KClO3,还原剂是P,结合方程式系数判断;
B、P2O5白色固体吸水性很强,吸收空气中的水分,生成磷酸小液滴;
C、磷元素化合价由0价升高为+5价,据此计算转移的电子数;
D、P2O5为酸性氧化物,也是磷酸的酸酐.
解答 解:A、反应5KClO3+6P═3P2O5+5KCl中,氧化剂是KClO3,还原剂是P,氧化剂和还原剂的物质的量之比为5:6,故A正确;
B、P2O5白色固体吸水性很强,极易吸收空气中的水分,生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾),同时含有氯化钾固体颗粒,所以产生的白色烟雾,故B正确;
C、反应5KClO3+6P═3P2O5+5KCl中,磷元素化合价由0价升高为+5价,消耗3molP时,转移电子的物质的量为3mol×5=15mol,故C正确;
D、P2O5为酸性氧化物,也是磷酸的酸酐,故D错误;
故选:D.
点评 本题考查学生氧化还原反应基本概念与计算、元素化合物的性质等,难度不大,掌握氧化还原反应有关基本概念.

练习册系列答案
相关题目
14.下列说法正确的是( )
| A. | 稀盐酸可除去烧瓶内残留的MnO2 | |
| B. | 稀硝酸可除去试管内壁的银镜 | |
| C. | Al2O3和MgO均可与NaOH溶液反应 | |
| D. | SO2和SO3混合气体通入Ba(NO3)2溶液可得到BaSO3和BaSO4 |
14.A元素的一个原子失去两个电子,转移到B元素的两个原子中去,形成化合物,下列说法正确的是( )
| A. | 该化合物的化学式为A2B | |
| B. | 该化合物的化学式为AB | |
| C. | 这种化合物中存在A2+和B3+两种微粒 | |
| D. | 这种化合物是离子化合物 |
11.下列图示与对应的叙述相符的是( )
| A. |  四种基本反应类型与氧化还原反应的关系 | |
| B. | 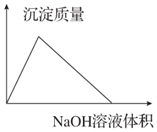 AlCl3溶液中滴加NaOH溶液生成沉淀的情况 | |
| C. |  Ba(OH)2溶液中滴加硝酸溶液导电性的情况 | |
| D. |  等体积等浓度稀硫酸分别与足量铁和镁反应的情况 |
8.下列离子方程式书写正确的是( )
| A. | 向Ba(OH)2溶液中加稀硫酸:Ba2++OH-+H++SO42?═BaSO4↓+H2O | |
| B. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 向小苏打溶液中加入少量的澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 足量CO2通入NaOH溶液:CO2+2 OH-═CO32-+H2O |
15.嫦娥二号卫星采用“长三丙火箭”进行发射,其第三级推进器使用的燃料是液态氢.已知在25℃时,2g H2(g)与O2(g)完全反应生成H2O(g)时放热241.8kJ.则下列有关判断正确的是( )
| A. | H2 (g)的燃烧热是-241.8 kJ/mol | |
| B. | 25℃时,H2(g)+$\frac{1}{2}$O2═H2O(1)△H>-241.8 kJ/mol | |
| C. | 25℃时,22.4 L H2完全燃烧生成H2O(g)放出的热量为241.8 kJ | |
| D. | 已知H2O(g)═H2O(1)△H=-44 kJ/mol.则H2O (1)═H2(g)+$\frac{1}{2}$O2(g)△H=+285.8 kJ/mol |
12.在某溶液M中加入物质X,物理量y与物质X体积的关系如图所示,下列有关溶液M、物质X和物理量y的推断合理的是( )


| 选项 | 溶液M | 物质X | 物理量y |
| A | 含Mg2+、Al3+、NH4+的溶液 | KOH溶液 | 沉淀的物质的量 |
| B | 含CO32-、HCO3-的溶液 | 盐酸 | 二氧化碳的体积 |
| C | 含OH-、AlO2-、SiO3 2-、CO32-的溶液 | NaHSO4溶液 | 沉淀的质量 |
| D | 含Ba(OH)2、NaOH、NaAlO2的溶液 | CO2 | 沉淀的物质的量 |
| A. | A | B. | B | C. | C | D. | D |
13.硝酸与金属反应往往产生氮氧化物,但是在某些特殊情况则不然.将稀硝酸(HNO3浓度低于2mol•L一1)与过量金属镁缓和反应放出一种无色无毒气体A,反应完全后向剩余溶液中加人过量NaOH固体并加热,放出气体B,将两次放出气体全部收集并混合,用碱石灰干燥后缓慢通过足量的灼热氧化铜固体,观察到固体变红,将剩余气体用浓硫酸干燥,最后气体体积变为原来的四分之三,则下列分析正确的是(本题中所有气体体积均为相同条件下测得的体积)( )
| A. | 无色无毒气体A为H2 | |
| B. | 最后气体为NH3 | |
| C. | 在镁与硝酸反应过程中还原剂与氧化剂的物质的量之比为5:1 | |
| D. | 气体A与气体B的体积比为1:1 |