题目内容
8.若用 NA表示阿伏加德罗常数的值,下列叙述不正确的是( )| A. | 在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.2 NA | |
| B. | l L 0.1mol•L-1的H2SO3溶液中含有H+的数目为0.2 NA | |
| C. | 7.8 g Na2O2中含有的阴离子数目为0.1 NA | |
| D. | 常温常压下,14 g乙烯和丙烯的混合气体中氢原子数为 2 NA |
分析 A、硫酸氢钠由1个钠离子和1个硫酸氢根构成;
B、亚硫酸是弱酸,在溶液中不能完全电离;
C、求出过氧化钠的物质的量,然后根据1mol过氧化钠中含2mol钠离子和1mol过氧根构成来分析;
D、乙烯和丙烯的最简式均为CH2.
解答 解:A、硫酸氢钠由1个钠离子和1个硫酸氢根构成,故0.1mol硫酸氢钠中含0.1mol钠离子和0.1mol硫酸氢根离子即共0.2mol即0.2NA个,故A正确;
B、亚硫酸是弱酸,在溶液中不能完全电离,故溶液中的氢离子的个数小于0.2NA个,故B错误;
C、7.8g过氧化钠的物质的量为0.1mol,而1mol过氧化钠中含2mol钠离子和1mol过氧根构成,故0.1mol过氧化钠中含0.1mol阴离子即0.1NA个,故C正确;
D、乙烯和丙烯的最简式均为CH2,故14g混合物中含有的CH2的物质的量为1mol,则含2mol氢原子即2NA个,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.铋(Bi)位于元素周期表中ⅤA族,其价态为+3价较稳定,铋酸钠(NaBiO3)溶液呈无色,取一定量的硫酸锰(MnSO4)溶液依次滴加下列溶液,对应的现象如下表所示:
则下列物质的氧化性由弱到强排列的顺序正确的是( )
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
| A. | I2,H2O2,KMnO4,NaBiO3 | B. | H2O2,I2,NaBiO3,KMnO4 | ||
| C. | NaBiO3,KMnO4,H2O2,I2 | D. | KMnO4,NaBiO3,I2,H2O2 |
20.用含有少量SiO2(酸性氧化物)的铝片制取纯净的氢氧化铝,有下列操作步骤,最恰当的组合是(按先后顺序排列)( )
①加盐酸溶解
②加过量烧碱溶液溶解
③过滤
④通入过量CO2生成Al(0H)3沉淀
⑤加入盐酸,生成Al(0H)3沉淀
⑥加入过量氨水溶液,生成Al(0H)3沉淀.
①加盐酸溶解
②加过量烧碱溶液溶解
③过滤
④通入过量CO2生成Al(0H)3沉淀
⑤加入盐酸,生成Al(0H)3沉淀
⑥加入过量氨水溶液,生成Al(0H)3沉淀.
| A. | ①③⑥③ | B. | ②③⑥③ | C. | ②③④③ | D. | ②③⑤③ |
17.某烃的一种同分异构体只能生成一氯代物,该烃的分子式不可以是( )
| A. | C3H6 | B. | C5H12 | C. | C6H14 | D. | C8H18 |
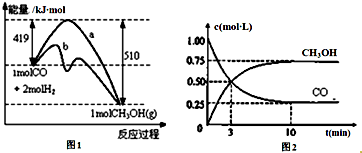 工业上用CO生产燃料甲醇.一定温度和容积条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.请回答下列问题:
工业上用CO生产燃料甲醇.一定温度和容积条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.请回答下列问题: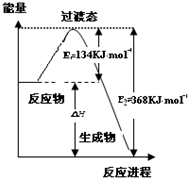 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.