题目内容
(22分)现有下列九种物质:
①H2 ②铝 ③CuO ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3
(1)按物质的分类方法填写表格的空白处:
分类标准 | 能导电 | 非电解质 | 电解质 |
属于该类的物质 |
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH-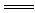 H2O,该离子反应对应的化学方程式为 。
H2O,该离子反应对应的化学方程式为 。
(3)⑨在水中的电离方程式为 ,
34.2g⑨溶于水配成250mL溶液, SO42-的物质的量浓度为 。
(4)少量的④通入⑥的溶液中反应的离子方程式为: 。
(5)将②加入NaOH的溶液中反应的离子方程式
(6)②与⑧发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是
(填化学式),还原剂与氧化剂的物质的量之比是 ,当有5.4g Al发生反应时,转移电子的物质的量为 。
19.(1) ②⑦⑧⑨ ④ ③⑤⑥⑨;(2)Ba(OH)2+2HNO3=Ba(NO3)2+2H2O
(3)Al2(SO4)3= 2Al3++3SO42- , 1.2mol/L
(4)Ba2++2OH-+CO2=BaCO3↓+H2O (5 ) 2Al+2OH-+2H2O=2AlO2-+3H2 ↑
(6)HNO3 1︰1 0.6mol 。
【解析】
试题分析:(1)能导电的物质必须是具有能自由移动的带电的微粒,金属能导电是由于金属中存在能自由移动的带负电的电子;水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物不管在水溶液中或熔融状态下能够导电与否,都不是电解质或非电解质,所以以上物质中能导电的是:②⑦⑧⑨,属于非电解质的是④,以上物质中属于电解质的是③⑤⑥⑨;
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH- H2O,该离子反应对应的化学方程式为Ba(OH)2+2HNO3=Ba(NO3)2+2H2O;
H2O,该离子反应对应的化学方程式为Ba(OH)2+2HNO3=Ba(NO3)2+2H2O;
(3)硫酸铝在水中的电离方程式为Al2(SO4)3= 2Al3++3SO42-,34.2g硫酸铝的物质的量为0.1mol, 溶于水配成250mL溶液, SO42-的物质的量浓度为(0.1/0.25)×3=1.2mol/L ;
(4)少量的二氧化碳通入氢氧化钡的溶液中反应的离子方程式为: Ba2++2OH-+CO2=BaCO3↓+H2O
(5)将铝加入NaOH的溶液中反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2 ↑
(6)根据氧化还原反应的概念,得电子,所含元素化合价降低的物质是氧化剂,硝酸是氧化剂,铝与硝酸得失电子均为3,还原剂与氧化剂的物质的量之比是1:1,5.4g Al的物质的量为5.4/27=0.2mol,发生反应时,转移电子的物质的量为0.6mol。
考点:考查电解质和非电解质的概念,能导电的物质等知识
