题目内容
4.下列离子方程式正确的是( )| A. | 氯气与水反应:Cl2+H2O?2H++Cl-+ClO- | |
| B. | 碳酸钡溶于醋酸:BaCO3+2H+═Ba2++H2O+CO2↑ | |
| C. | 金属钠跟水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 澄清石灰中通入过量二氧化碳:Ca2++2OH-+CO2═CaCO3↓+H2O |
分析 A.反应生成的HClO在离子反应中保留化学式;
B.醋酸在离子反应中保留化学式;
C.反应生成NaOHH和氢气,电子、电荷守恒;
D.反应生成碳酸氢钙.
解答 解:A.氯气与水反应的离子反应为Cl2+H2O?H++Cl-+HClO,故A错误;
B.碳酸钡溶于醋酸:BaCO3+2CH3COOH═2CH3COO-+Ba2++H2O+CO2↑,故B错误;
C.金属钠跟水反应的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故C正确;
D.澄清石灰中通入过量二氧化碳的离子反应为OH-+CO2═HCO3-,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
15.在一定条件下,可以用如图(1)所示的硼化钒(VB2)-空气电池(工作时反应为:4VB2+11O2═4B2O3+2V2O5)为电源给图(2)所示装置通电,模拟有机物的电化学储氢.下列说法正确的是( )
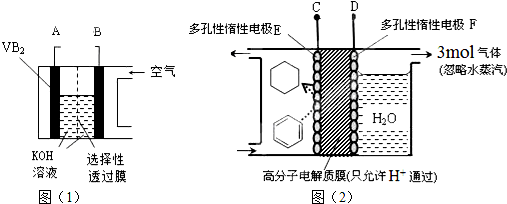

| A. | 整套装置工作时的连接为A连接D、B连接C | |
| B. | VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O | |
| C. | 电极F产生3mol气体时电极E得到的氧化产物为2mol | |
| D. | 储氢装置工作时,右侧电极区的pH值减小2×10-9 |
12.下列反应的离子方程式书写正确的是( )
| A. | 铝片放入氢氧化钠溶液中:Al+2OH-═AlO${\;}_{2}^{-}$+H2↑ | |
| B. | Na与水反应:Na+2H2O═Na++H2↑+2OH- | |
| C. | 向AlCl3溶液中加入过量NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | AlCl3溶液中滴入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ |
19.下列有机物中,既能发生加成反应、酯化反应,又能发生氧化反应的是( )
①CH2OH(CHOH)4CHO
②CH3CH2CH2OH
③CH2═CH-CH2OH
④CH2═CH-COOCH3
⑤CH2═CH-COOH.
①CH2OH(CHOH)4CHO
②CH3CH2CH2OH
③CH2═CH-CH2OH
④CH2═CH-COOCH3
⑤CH2═CH-COOH.
| A. | ③⑤ | B. | ②④ | C. | ①③⑤ | D. | ①③ |
8.科学研究发现,具有高度对称性的有机分子具有致密性高,稳定性强,张力能大等特点,因此这些分子成为2014年化学界关注的热点,下面是几种常见高度对称烷烃的分子碳架结构这三种烷烃的二氯取代产物的同分异构体数目是( )
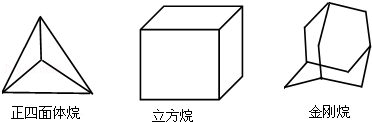

| A. | 2种 4种 8种 | B. | 2种 4种 6种 | C. | 1种 3种 6种 | D. | 1种 3种 8种 |
 ④CH3COOH⑤HOCH2CHO ⑥CH3CH2CH2CH3⑦葡萄糖 ⑧蛋白质⑨淀粉
④CH3COOH⑤HOCH2CHO ⑥CH3CH2CH2CH3⑦葡萄糖 ⑧蛋白质⑨淀粉
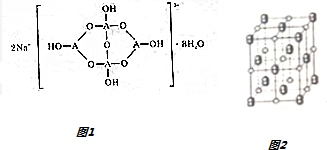

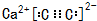 ,若晶胞的长、宽、高分别为520pm、520pm和690pm,则该晶体的密度为2.28g/cm3(精确至0.01)
,若晶胞的长、宽、高分别为520pm、520pm和690pm,则该晶体的密度为2.28g/cm3(精确至0.01)