题目内容
6.下列物质中.溶于水后溶液呈碱性的是( )| A. | NO2 | B. | NaCl | C. | Na2S | D. | Na2O2 |
分析 A.二氧化氮和水反应生成硝酸显酸性;
B.氯化钠溶于水得到氯化钠溶液,溶液呈中性;
C.硫化钠溶于水,溶液中硫离子水解溶液呈碱性;
D.过氧化钠和水反应生成氢氧化钠显碱性.
解答 解:A.3NO2+H2O=2HNO3+NO,HNO3=H++NO3-,硝酸是酸,电离出氢离子,所以溶液呈酸性,故A错误;
B.氯化钠溶于水得氯化钠溶液,NaCl=Na++Cl-,所以溶液呈中性,故B错误;
C.Na2S溶于水形成的溶液中,硫离子水解,S2-+H2O?HS-+OH-,所以溶液呈碱性,故C正确;
D.过氧化钠(Na2O2)和水反应,2Na2O2+2H2O=4NaOH+O2↑,能生成氢氧化钠,所以溶液呈碱性,故D正确;
故选CD.
点评 本题考查溶液酸碱性的判断,根据溶液中电解质的性质来分析解答即可,题目难度不大.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
16.现有五种元素,其中A、B、C为短周期主族元素,D、E为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)A基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形形.
(2)E在周期表的位置是第四周期第IB族,位于ds区,其基态原子有29种运动状态.
(3)BC3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形,检验D元素的方法是焰色反应.
(4)E单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示.则晶胞中该原子的配位数为12,E单质晶体中原子的堆积方式为四种基本堆积方式中的面心立方堆积.若已知E的原子半径为d cm,NA代表阿伏加德罗常数,E的相对原子质量为M,则该晶体的密度为$\frac{M}{4\sqrt{2}{d}^{3}{N}_{A}}$g•cm-3(用字母表示).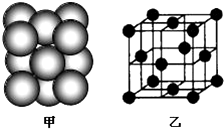
| A元素原子的核外p电子总数比s电子总数少1 |
| B原子核外所有p轨道全满或半满 |
| C元素的主族序数与周期数的差为4 |
| D是前四周期中电负性最小的元素 |
| E在周期表的第十一列 |
(2)E在周期表的位置是第四周期第IB族,位于ds区,其基态原子有29种运动状态.
(3)BC3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形,检验D元素的方法是焰色反应.
(4)E单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示.则晶胞中该原子的配位数为12,E单质晶体中原子的堆积方式为四种基本堆积方式中的面心立方堆积.若已知E的原子半径为d cm,NA代表阿伏加德罗常数,E的相对原子质量为M,则该晶体的密度为$\frac{M}{4\sqrt{2}{d}^{3}{N}_{A}}$g•cm-3(用字母表示).

14.下列变化不属于化学变化的是( )
| A. | 石油分馏 | B. | 煤的干馏 | C. | 钢铁生锈 | D. | 煤的液化 |
1.有关下列能量转化的认识不正确的是( )
| A. | 植物的光合作用使得太阳能转化为了化学能 | |
| B. | 燃料燃烧时只是将化学能转化为了热能 | |
| C. | 生物体内的化学变化过程在能量转化上比在体外发生的一些能量转化更为合理、有效 | |
| D. | 人类使用照明设备是将电能转化为了光能 |
11.下列实验方法能达到实验目的是( )
| A. | 用排水集气法收集氨气 | |
| B. | 用分液漏斗分离水与乙醇的混合物 | |
| C. | 用淀粉溶液检验溶液中是否存在碘单质 | |
| D. | 用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液 |
16.下列实验操作,不能用以分离提纯物质的是( )
| A. | 萃取 | B. | 称量 | C. | 蒸馏 | D. | 蒸发 |