题目内容
在反应2KMnO4A.K2MnO4 B.MnO2 C.O2 D.KMnO4
AB
解析:还原产物是氧化剂发生还原反应得到的产物,在上述反应中锰元素化合价由+7降到+6、+4两种价态。因此K2MnO4和MnO2均为还原产物。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
近日来,质检部门在众多品牌乳制品中检出有毒有机物三聚氰胺[C3N3(NH2)3],在乳制品行业掀起了一场轩然大波,引发了一场关于食品安全问题的大讨论.三聚氰胺是一种重要的有机化工原料,因其含氮量高而被不法商家用作食品添加剂,以提升食品检测中的蛋白质含量指标(N%),因此三聚氰胺也被人称为“蛋白精”.三聚氰胺遇强酸或强碱水溶液水解,胺基逐步被羟基取代,最后生成三聚氰酸[C3N3(OH)3].三聚氰酸可用于消除汽车尾气中的NO2.其反应原理为:C3N3(OH)3
3HNCO; 8HNCO+6NO2
7N2+8CO2+4H2O,下列说法正确的是( )
| ||
| ||
| A、C3N3(OH)3与HNCO为同一物质 |
| B、HNCO是一种很强的氧化剂 |
| C、1mol NO2在反应中转移的电子为4mol |
| D、反应中NO2是还原剂 |
随着材料科学的发展,金属钒被誉为“合金的维生素”.为回收利用含钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺.
己知:V可形成VO2+、VO2+、VO3-等多种离子;部分含钒物质在水中的溶解性如下表所示:
该工艺的主要流程如下:
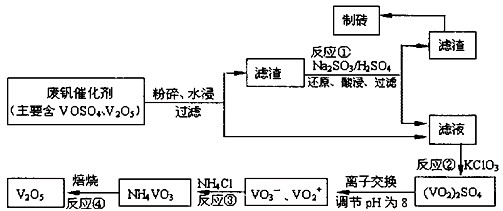
请回答下列问题
(1)工业上常用铝热反应法由V2O5冶炼金属钒,请写出反应的化学方程式 .
(2)反应①的离子方程式是 .
(3)在反应②中,每生成1mol(VO2)2SO4转移电子的数目为 .
(4)在离子交换过程中,发生可逆反应VO2++2OH-?VO3-+H2O.
该反应的化学平衡常数K 的表达式为 .
(5)反应③充分反应后,分离出NH4VO3的实验所需主要玻璃仪器为 ,为保证产品纯度,还应进行的操作名称是 .
己知:V可形成VO2+、VO2+、VO3-等多种离子;部分含钒物质在水中的溶解性如下表所示:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |

请回答下列问题
(1)工业上常用铝热反应法由V2O5冶炼金属钒,请写出反应的化学方程式
(2)反应①的离子方程式是
(3)在反应②中,每生成1mol(VO2)2SO4转移电子的数目为
(4)在离子交换过程中,发生可逆反应VO2++2OH-?VO3-+H2O.
该反应的化学平衡常数K 的表达式为
(5)反应③充分反应后,分离出NH4VO3的实验所需主要玻璃仪器为

 I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,
I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中, 2X
2X 2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是
2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是


 用如图的实验装置可以进行钠跟水的反应实验,并可收集、检验生成的气体.Na的密度为0.97g/mL,煤油的密度为0.87g/mL,请回答下列问题:
用如图的实验装置可以进行钠跟水的反应实验,并可收集、检验生成的气体.Na的密度为0.97g/mL,煤油的密度为0.87g/mL,请回答下列问题: