题目内容
16.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 使甲基橙变红的溶液:Fe2+、K+、SO42-、NO3- | |
| B. | 中性溶液中:Fe3+、Na+、NO3-、Cl- | |
| C. | 0.1mol•L-1NaAlO2溶液:K+、OH-、Cl-、NO3- | |
| D. | 水电离出的c(H+)=10-12mol•L-1的溶液:Na+、K+、NH4+、[Ag(NH3)2]+ |
分析 A.使甲基橙变红的溶液为酸性溶液中,溶液中存在电离氢离子,硝酸根离子在酸性条件下能够氧化亚铁离子;
B.铁离子只能存在于中性溶液中;
C.四种离子之间不反应,都不与偏铝酸钠反应;
D.水电离出的c(H+)=10-12mol•L-1的溶液中存在电离氢离子或氢氧根离子,[Ag(NH3)2]+与氢离子反应,铵根离子与氢氧根离子反应.
解答 解:A.使甲基橙变红的溶液为酸性溶液中,Fe2+、NO3-在酸性条件下发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.Fe3+只能存在于中性溶液,中性溶液中会生成氢氧化铁沉淀,故B错误;
C.K+、OH-、Cl-、NO3-之间不发生反应,都不与NaAlO2反应,在溶液中能够大量共存,故C正确;
D.水电离出的c(H+)=10-12mol•L-1的溶液为酸性或碱性溶液,溶液中存在电离氢离子或氢氧根离子,[Ag(NH3)2]+与氢离子反应,NH4+与氢氧根离子反应,在溶液中一定不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的正误判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
7.下列有关物质的鉴别方案错误的是( )
| A. | 用澄清石灰水鉴别氮气和二氧化碳 | |
| B. | 用肥皂水鉴别硬水和软水 | |
| C. | 用闻气味的方法鉴别白酒和白醋 | |
| D. | 用稀盐酸鉴别碳酸钠粉末和碳酸钙粉末 |
4.下列说法正确的是( )
| A. | 1mol H2O2中含有18NA个电子 | |
| B. | 阿伏加德罗常数的符号为NA,NA≈6.02×1023 | |
| C. | 阿伏加德罗常数是0.012kg C中所含的碳原子数 | |
| D. | 1mol OH-的质量为17g/mol |
11.下列陈述 I、II正确并且有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | 锌金属活动性比铁强 | 海轮外壳上装锌块可减缓腐蚀 |
| B | Ba(OH)2可与盐酸反应 | Ba(OH)2可用于治疗胃酸过多 |
| C | SiO2是酸性氧化物 | SiO2能与水反应生成硅酸 |
| D | H2O2有氧化性 | H2O2能使酸性高锰酸钾溶液褪色 |
| A. | A | B. | B | C. | C | D. | D |
1. 重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断PM2.5待测试样的pH约为4.
(2)为减少SO2的排放,常采取的措施有:将煤转化为清洁气体燃料.
已知:①2H2(g)+O2(g)═2H2O(g)K1 ②2C(s)+O2(g)═2CO(g)K2
C(s)+H2O(g)=CO(g)+H2(g) K=$(\frac{{K}_{1}}{{K}_{2}})^{\frac{1}{2}}$(用含K1、K2的式子表示).
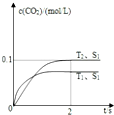
(3)汽车尾气净化的主要原理为:2NO(g)+2CO(g)?2CO2(g)+N2(g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示.
①在T2温度下,0~2s内的平均反应速率υ(N2)=0.025mol/(L•s).
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2,在如图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线.
(4)①已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0,若1mol空气含0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡,测得NO为8×10-4mol.计算该温度下的平衡常数K=4×10-6.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)已知该反应的△H>0,简述该设想能否实现的依据:不能实现,因为该反应是焓增、熵减的反应,△G=△H-T•△S>0.
 重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:(1)将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)为减少SO2的排放,常采取的措施有:将煤转化为清洁气体燃料.
已知:①2H2(g)+O2(g)═2H2O(g)K1 ②2C(s)+O2(g)═2CO(g)K2
C(s)+H2O(g)=CO(g)+H2(g) K=$(\frac{{K}_{1}}{{K}_{2}})^{\frac{1}{2}}$(用含K1、K2的式子表示).
(3)汽车尾气净化的主要原理为:2NO(g)+2CO(g)?2CO2(g)+N2(g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示.
①在T2温度下,0~2s内的平均反应速率υ(N2)=0.025mol/(L•s).
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2,在如图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线.
(4)①已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0,若1mol空气含0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡,测得NO为8×10-4mol.计算该温度下的平衡常数K=4×10-6.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)已知该反应的△H>0,简述该设想能否实现的依据:不能实现,因为该反应是焓增、熵减的反应,△G=△H-T•△S>0.
8.下列碱中,碱性最强的是( )
| A. | 氢氧化钾 | B. | 氢氧化钠 | C. | 氢氧化镁 | D. | 氢氧化铝 |
5.下列有机反应中属于消去反应的是( )
| A. | 苯与浓硫酸、浓硝酸在60℃下共热 | |
| B. | 乙醇与浓硫酸共热,温度保持在170℃ | |
| C. | 银氨溶液中滴入乙醛,热水浴温热 | |
| D. | 冰醋酸、乙醇、浓硫酸混合均匀加热 |
6.关于SiO2的叙述中,错误的是( )
| A. | SiO2和CO2都是酸性氧化物,都能与强碱溶浓反应 | |
| B. | SiO2和CO2都能溶于水且与水反应生成相应的酸 | |
| C. | 工艺师利用HF溶液刻蚀石英制作艺术品 | |
| D. | 除去SiO2中混有的CaCO3可加入适量的稀盐酸,然后过滤 |