题目内容
11.下列陈述 I、II正确并且有因果关系的是( )| 选项 | 叙述I | 叙述II |
| A | 锌金属活动性比铁强 | 海轮外壳上装锌块可减缓腐蚀 |
| B | Ba(OH)2可与盐酸反应 | Ba(OH)2可用于治疗胃酸过多 |
| C | SiO2是酸性氧化物 | SiO2能与水反应生成硅酸 |
| D | H2O2有氧化性 | H2O2能使酸性高锰酸钾溶液褪色 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Zn、Fe形成原电池,Fe作正极;
B.钡离子有毒;
C.二氧化硅难溶于水;
D.高锰酸钾与H2O2反应,H2O2作还原剂.
解答 解:A.Zn、Fe形成原电池,锌金属活动性比铁强,Zn作负极被腐蚀,Fe作正极被保护,所以海轮外壳上装锌块可减缓腐蚀,故A正确;
B.钡离子有毒,所以不能用氢氧化钡来治疗胃酸过多,故B错误;
C.二氧化硅难溶于水,二氧化硅与水不反应,不能用SiO2与水反应生成硅酸,故C错误;
D.高锰酸钾与H2O2反应,高锰酸钾作氧化剂,H2O2作还原剂,H2O2表现还原性,故D错误.
故选A.
点评 本题考查了物质的性质,熟悉浓原电池原理、钡离子的性质、氧化还原反应等知识点是解题关键,题目难度不大.

练习册系列答案
相关题目
6.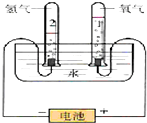 水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.
水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.
(1)写出电解水的化学方程式,若为氧化还原反应,请用双线桥表示出电子的转移方向和数目.
 .
.
(2)假设电解了3.6gH2O,请完成下表.
(3)若在47.8gH2O(过量)中加入2.3gNa.钠与水反应的离子方程式为2Na+2 H2O═2Na++2OH-+H2↑,,反应后得到的溶液中溶质是NaOH,溶质的质量分数为8%,若要计算该溶液中溶质的物质的量浓度,则还需要溶液密度(填物理量).
(4)若在电解水后收集到O2体积为22.4mL(在标准状况下),则收集到的H2的质量0.004g.
 水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.
水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.(1)写出电解水的化学方程式,若为氧化还原反应,请用双线桥表示出电子的转移方向和数目.
 .
.(2)假设电解了3.6gH2O,请完成下表.
| 质 量 | 物质的量 | O2与H2的体积比(同温同压下) | |
| O2 | 3.2g | 0.1mol | 1:2 |
| H2 | 0.4g | 0.2mol |
(4)若在电解水后收集到O2体积为22.4mL(在标准状况下),则收集到的H2的质量0.004g.
16.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红的溶液:Fe2+、K+、SO42-、NO3- | |
| B. | 中性溶液中:Fe3+、Na+、NO3-、Cl- | |
| C. | 0.1mol•L-1NaAlO2溶液:K+、OH-、Cl-、NO3- | |
| D. | 水电离出的c(H+)=10-12mol•L-1的溶液:Na+、K+、NH4+、[Ag(NH3)2]+ |
3.全钒液流电池是一种新型的绿色环保储能电池.其电池总反应为:V3++VO2++H2O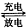 VO2++2H++V2+..下列说法正确的是( )
VO2++2H++V2+..下列说法正确的是( )
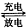 VO2++2H++V2+..下列说法正确的是( )
VO2++2H++V2+..下列说法正确的是( )| A. | 放电时正极反应为:VO${\;}_{2}^{+}$+2H++e-═VO2++H2O | |
| B. | 充电过程中,H+由阴极区向阳极区迁移 | |
| C. | 放电过程中电子由负极经外电路移向正极,再由正极经电解质溶液移向负极 | |
| D. | 充电时阴极反应为:V2+-e-═V3+ |
20.0.02mol•L-1的HCN溶液与0.02mol•L-1 NaCN溶液等体积混合,已知混合溶液中c(CN-)<c(Na+),则下列关系中,正确的是( )
| A. | c(Na+)>c(CN-)>c(H+)>c(OH-) | B. | c(HCN)+c(CN-)═0.04 mol•L-1 | ||
| C. | c(Na+)+c(H+)═c(CN-)+c(OH-) | D. | c(CN-)<c(HCN) |
1.用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 23g Na完全转化生成Na2O和Na2O2,失去电子数为NA 到2NA之间 | |
| B. | 常温常压下,46g由NO2和N2O4组成的混合气体中含有原子的总数为3NA | |
| C. | 含2mol H2SO4的浓硫酸与足量铜微热反应,生成SO2分子数为NA | |
| D. | 粗铜精炼时转移1mol电子,阳极上溶解的Cu原子数一定为0.5 NA |