题目内容
12.(1)标准状况下,11.2L某气体的质量为14g,则其摩尔质量为28g/mol.(2)含0.4molAl3+的Al2(SO4)3中所含的SO42-的物质的量是0.6mol.
(3)从2mol/L的氯化铜溶液中取出0.8molCl-,需要氯化铜溶液的体积为0.2L.
(4)一定温度和压强下,m g摩尔质量为M g/mol的某气体体积为v L,则在该条件下的气体摩尔体积为$\frac{VM}{m}$L/mol.
分析 (1)根据M=$\frac{m}{\frac{V}{V{\;}_{m}}}$计算;
(2)根据Al2(SO4)3中Al3+:SO42-=2:3求SO42-物质的量;
(3)根据体积V=$\frac{n}{c}$计算;
(4)根据Vm=$\frac{V}{n}$=$\frac{V}{\frac{m}{M}}$计算.
解答 解:(1)根据M=$\frac{m}{\frac{V}{V{\;}_{m}}}$=$\frac{14}{\frac{11.2}{22.4}}$=28g/mol,故答案为:28g/mol;
(2)因为Al2(SO4)3中Al3+:SO42-=2:3,所以含0.4molAl3+的Al2(SO4)3中所含的SO42-的物质的量是$\frac{0.4}{2}$×3=0.6mol,故答案为:0.6mol;
(3)从2mol/L的氯化铜溶液中取出0.8molCl-,即取出0.4mol氯化铜,所以V=$\frac{n}{c}$=$\frac{0.4}{2}$=0.2L,故答案为:0.2L;
(4)因为Vm=$\frac{V}{n}$=$\frac{V}{\frac{m}{M}}$=$\frac{VM}{m}$L/mol,故答案为:$\frac{VM}{m}$L/mol.
点评 本题考查关系式,求物质的摩尔质量和物质的量以及根据关系式求气体的体积等,比较容易.

练习册系列答案
相关题目
3. 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | a点对应的溶液中:Na+、AlO2-、SO42-、NO3- | |
| B. | b点对应的溶液中:Ba2+、K+、NO3-、Cl- | |
| C. | c点对应的溶液中:Na+、Ag+、Mg2+、NO3- | |
| D. | d点对应的溶液中:Cl-、NO3-、Fe2+、Na+ |
7.下列说法不正确的是( )
| A. | 磷酸的摩尔质量与NA个硫酸分子的质量在数值上相等 | |
| B. | 6.02×1023个氮分子和6.02×l023个氢分子的质量比等于14:1 | |
| C. | 32g氧气所含的原子数目约为2×6.02×1023 | |
| D. | 标准状况下,0.5NA分氟化氢分子所占体积是11.2L |
17.下列分类标准正确的是( )
| A. | 化学反应分为:氧化还原反应、非氧化还原反应(标准:有没有单质参加或生成) | |
| B. | 分散系分为:溶液、胶体、浊液(标准:有没有丁达尔效应) | |
| C. | 化学反应分为:化合反应、分解反应、置换反应、复分解反应(标准:按反应物和生成物的类别以及反应前后物质种类的多少) | |
| D. | 无色的溶液:CO32-、SO42-、Cu2+、NH4+ |
1.已知H2SO4(aq)与Ba(OH)2(aq)反应的△H=-1584.2kJ/mol;HCl(aq)与NaOH(aq)反应的△H=-55.6kJ/mol.则生成BaSO4(s)的反应热等于( )
| A. | -1528.6kJ/mol | B. | -1473kJ/mol | C. | +1473kJ/mol | D. | +1528.6kJ/mol |
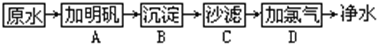
 铁及其化合物与生产、生活关系密切,请回答下列问题:
铁及其化合物与生产、生活关系密切,请回答下列问题: